Боли в суставах, чувство «скованности» с утра. Что это? Переутомились на работе? «Перезанимались» в спортзале? Простудились?
Перечисленные выше проявления могут свидетельствовать о недуге, причина которого и на сегодняшний день остается не до конца понятной.
Ревматоидный артрит. О нем мы говорим с кандидатом медицинских наук, врачом-ревматологом «Клиника Эксперт Воронеж» Стрельниковой Инной Алексеевной.
— Инна Алексеевна, что такое ревматоидный артрит и по каким причинам возникает это заболевание?
Это иммуновоспалительное ревматическое заболевание неизвестной этиологии. Характеризуется хроническим эрозивным артритом и системным поражением внутренних органов.
Причины ревматоидного артрита на сегодняшний день медицине до конца неизвестны. По данным мировой статистики им страдает в среднем около 1% населения.
— Ревматоидный артрит кодируется в МКБ-10?
Да. Он отражен под кодом M05 (серопозитивный ревматоидный артрит) и M06 (другие ревматоидные артриты).
— Что происходит с организмом при ревматоидном артрите?
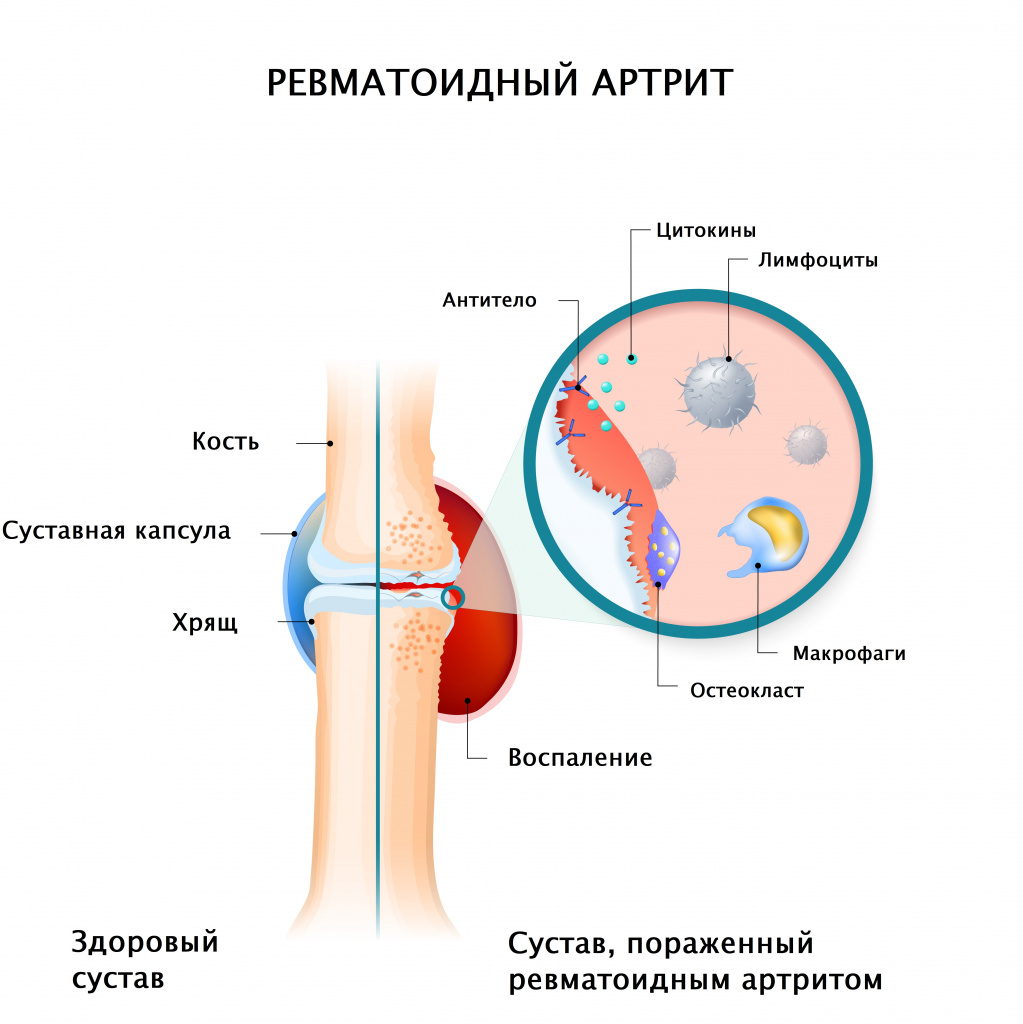
В основе развития данного заболевания — воспаление иммунной природы, преимущественно затрагивающее ткани суставов.
На начальных стадиях пациент предъявляет жалобы на боли и припухлость в суставах, на утреннюю скованность более 30 минут. Наиболее часто поражаются мелкие суставы кистей и стоп.
Для этой патологии также характерны внесуставные проявления. К ним относятся васкулиты кожи и других органов, нейропатии, плевриты, синдром Шегрена, ревматоидные узелки.
При ревматоидном артрите иногда отмечаются так называемые конституциональные признаки: общая слабость, снижение массы тела, повышение температуры тела. Но этих признаков может и не быть.
— Это заболевание подкрадывается незаметно или у ревматоидного артрита есть предвестники?
Предвестники есть не всегда. Заболевание может начаться сразу с классических проявлений. Однако зачастую на протяжении года могут отмечаться неспецифические жалобы на боли в суставах. Боли меняют свою локализацию (т.е. то в одном, то в другом суставе), либо отмечаются одновременно в нескольких, симметрично или не симметрично. Также могут отмечаться «скованность», припухание суставов (необязательно). На этом этапе ставится диагноз «недифференцированный артрит».
Что такое артрит и как его диагностировать? Рассказывает Мациев Дэниз Русланович – врач-рентгенолог
«МРТ Эксперт Сочи»
Как самостоятельное проявление, без суставных признаков, может повышаться скорость оседания эритроцитов (СОЭ), увеличивается содержание С-реактивного белка (лабораторные признаки воспаления). Здесь также могут отмечаться конституциональные проявления, о которых я говорила.
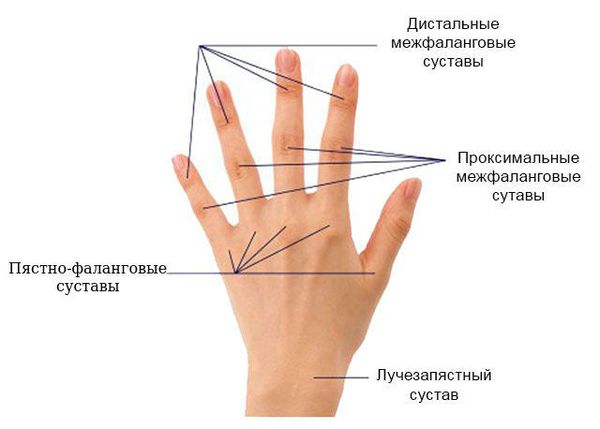
— Какие суставы чаще поражает ревматоидный артрит?
Определенные мелкие суставы кистей и стоп (пястно- и плюстне-фаланговые, проксимальные межфаланговые суставы кистей и стоп). Значительно реже затрагиваются крупные суставы: тазобедренные, коленные, лучезапястные, плечевые.
— Что входит в стандарт диагностики ревматоидного артрита?
Собираются жалобы, подробный анамнез, проводится тщательный осмотр, объективное обследование пациента.
Обязательно выполняются лабораторные исследования. К ним относится общий анализ крови, общий анализ мочи, анализ крови на С-реактивный белок, ревматоидный фактор, антитела к циклическому цитруллинированному пептиду (АЦЦП).
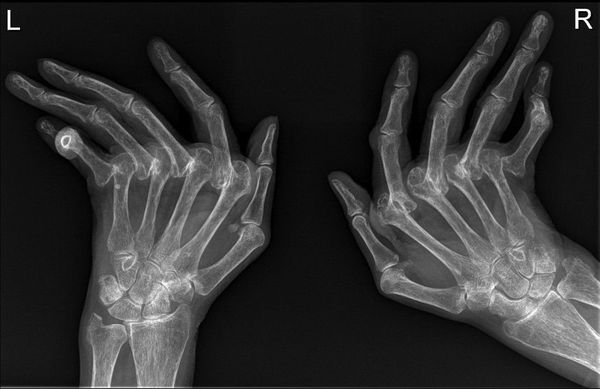
Также выполняется рентгенография суставов кистей и/или стоп, а также любых других суставов, со стороны которых имеются явные проявления.
Опасен ли рентген? Рассказывает Юлия Александровна Руцкая – заведующая отделением лучевой диагностики
«Клиники Эксперт Курск»
По показаниям может выполняться рентгенография или компьютерная томография органов грудной клетки, электрокардиография и другие исследования.
— Чем отличается ревматизм, ревматоидный артрит и полиартрит?
Понятие «ревматизм» в современной медицине уже не используются. Вместо него приняты обозначения «острая ревматическая лихорадка» и «ревматическая болезнь сердца».
Острая ревматическая лихорадка встречается чаще у молодых людей, чаще женского пола (от 7 до 25 лет). Начинается с ангины (острый период). Спустя 2-3 недели появляются боли в суставах, боли в сердце, может быть кольцевидная эритема, хорея.
Острая ревматическая лихорадка может протекать без формирования порока сердца или с ним. В последнем случае говорят о ревматической болезни сердца. Если порок не образуется, ревматическая лихорадка обычно проходит, повторы ее встречаются крайне редко. На сегодняшний день эта патология встречается реже.
Что касается полиартрита — уже по названию можно сделать вывод, что речь идет о воспалительном поражении нескольких суставов. Полиартрит может быть ревматоидным, псориатическим и т.д. Т.е. это не самостоятельный диагноз, а скорее синдром.
— У кого чаще возникает ревматоидный артрит: у мужчин или у женщин?
У женщин. Дебют заболевания — чаще от 40 до 55 лет (реже — в более молодом и более позднем возрасте). Соотношение к мужчинам по частоте — 3:1.
Почему остеопороз называют женской болезнью? Читать далее
— Этот диагноз может быть у детей?
Да. Он формулируется как «ювенильный ревматоидный артрит».
— Кто находится в группе риска по развитию ревматоидного артрита?
Это лица, у которых, при полном отсутствии симптомов заболевания, в крови имеется повышенный уровень ревматоидного фактора, АЦЦП. Такая картина может наблюдаться в течение нескольких лет. Само заболевание при этом может и не развиться.
В остальном выделение группы риска проблематично. Наследственность и фактор предрасположенности до конца не изучены.
Провоцирующим фактором (не фактором риска возникновения) могут быть переохлаждение, перенесенная инфекция.
— Врачи какой специальности занимаются лечением больных с ревматоидным артритом?
Преимущественно ревматологи.
Ликбез по врачебным профессиям. Когда обращаться к ревматологу? Рассказывает врач-ревматолог
«Клиника Эксперт Тверь» Масюков Семён Андреевич
В удаленных районах, где таких специалистов нет, больных могут лечить терапевты и врачи общей практики, но с периодическими консультациями ревматологов. Однако все же лучше, чтобы такими пациентами занимался ревматолог.
Записаться к врачу-ревматологу можно здесь
внимание: консультации доступны не во всех городах
При необходимости к лечению подключаются ортопеды, неврологи и др.
— Это заболевание можно вылечить раз и навсегда или этот серьёзный диагноз – приговор?
Ревматоидный артрит — это не приговор. На вопрос, излечим ли он или нет, ответ есть. При правильном лечении можно добиться низкой активности заболевания или полной ремиссии на определенный период времени. Лечение проводится пожизненно.
— Ревматоидный артрит и гормональное лечение – это синонимы или возможна терапия без применения гормоносодержащих препаратов?
Лечение без гормональных препаратов возможно. В идеале оно не применяется совсем, либо такие средства используются местно (в частности, внутрисуставная инъекция).
В иных случаях такие препараты могут назначаться системно (например в виде таблеток) — при дебюте заболевания, при выраженной активности воспаления. В последующем их отменяют. В отдельных случаях небольшие дозировки гормонов используются постоянно.
— Каковы последствия ревматоидного артрита?
При отсутствии правильного лечения и значительной активности воспалительного процесса — ранняя инвалидизация, деформации суставов, повышенный риск инфекционных заболеваний. При вовлечении в процесс внутренних органов (сердечно-сосудистая, легочная патология и т.д.) — снижение продолжительности жизни.
Что такое тахикардия и по каким причинам она возникает? Рассказывает врач-кардиолог
ООО «Клиника Эксперт Курск» Новикова Елена Викторовна
— Ревматоидный артрит накладывает ограничения на образ жизни больного? Что можно и что нельзя делать при этой болезни?
При низкой активности процесса или в стадии ремиссии возможны регулярные легкие физические нагрузки, катание на велосипеде, плавание. Рекомендуется рационально питаться, соблюдать режим труда и отдыха. При отсутствии деформации суставов особых ограничений нет.
Следует избегать переохлаждения, инфекционных заболеваний. Нежелательны чрезмерные физические нагрузки: ревматоидный артрит и спорт высоких достижений — вещи, на мой взгляд, несовместимые. Это может привести к усугублению течения ревматоидного артрита.
Не допускать избыточного веса, отказаться от курения. При какой-либо активности процесса не следует посещать сауны и бани.
Могла ли помочь МРТ суставов Микеланджело? Узнать здесь
— Расскажите о профилактике ревматоидного артрита. Как не спровоцировать обострение заболевания?
Поскольку причина заболевания не изучена, первичной профилактики не существует.
Профилактика рецидивов ревматоидного артрита включает в себя постоянное выполнение рекомендаций ревматолога по лечению; отказ от курения; избегание переохлаждений, инфекций, чрезмерных физических нагрузок; поддержание нормальной массы тела.
Для справки:
Стрельникова Инна Алексеевна
Выпускница лечебного факультета Воронежской государственной медицинской академии 2007 года.
В 2008 году окончила клиническую интернатуру по специальности «Терапия».
С 2008 по 2011 год проходила очную аспирантуру по специальности «Внутренние болезни». Имеет ученую степень кандидата медицинских наук.
В 2009 году прошла первичную специализацию по ревматологии.
С 2015 года и по настоящее время работает на должности врача-ревматолога в ООО «Клиника Эксперт Воронеж». В Воронеже принимает по адресу: г. Воронеж, ул. Пушкинская, дом № 11.
- ИНВИТРО
- Библиотека
- Справочник заболеваний
- Ревматоидный артрит
Ревматоидный артрит
Ревматоидный артрит: причины появления, симптомы, диагностика и способы лечения.
Определение
Ревматоидный артрит – хроническое, нередко приводящее к инвалидизации аутоиммунное заболевание суставов с развитием эрозивного артрита и системного поражения внутренних органов.
Чаще ревматоидным артритом страдают женщины, однако заболевание встречается и у мужчин.
Ревматоидный артрит может развиться в любом возрасте, даже у детей и подростков (ювенильный ревматоидный артрит). Заболевание наиболее распространено в возрастной группе старше 40 лет.
Причины ревматоидного артрита
Точные причины развития ревматоидного артрита не известны. Наиболее популярной является полиэтиологическая теория влияния на организм множества патологических факторов. В научном сообществе активно изучаются такие инфекционные пусковые механизмы (например, вирус Эпштейна–Барр и парвовирус В19), курение, воздействие белков иммунитета человека на собственные ткани.
Считается, что курение, прием оральных контрацептивов, а также злоупотребление кофеином осложняют течение ревматоидного артрита.
Далеко не последнюю роль в развитии заболевания суставов играют наследственные факторы. В настоящее время доказано, что риск заболеть ревматоидным артритом в 1,5 раза больше у родственников первой линии родства, чем у людей, не имеющих близких родственников, страдающих этим заболеванием.
Развитие ревматоидного артрита ассоциировано с носительством антигена HLA-DR4 (или DR1), который включает в себя более 22 аллелей (различных форм одного и того же гена). Характерная последовательность аминокислот в этих генах получила название «общий эпитоп», или иначе shared epitops – SE. Предполагают, что SE активирует Т-лимфоциты (клетки иммунного ответа) и направляет их агрессию против тканей собственного организма.
Носительство SE связано с тяжелым течением ревматоидного артрита и быстрым прогрессированием повреждения суставов.
Повышается риск развития внесуставных осложнений ревматоидного артрита, таких как воспаление сосудов, и интерстициальных заболеваний легочной ткани.
Под воздействием как внешних, так и внутренних факторов возникает аутоиммунное воспаление, основная агрессия которого направлена на синовиальную (внутреннюю) оболочку сустава. Этот процесс неумолимо прогрессирует и без должного лечения приводит к разрушению суставного хряща и кости.
Классификация ревматоидного артрита
Ревматоидный артрит в зависимости от обнаруженных в крови серологических маркеров подразделяют на серопозитивный и серонегативный.
К особым клиническим формам ревматоидного артрита относят:
- синдром Фелти – ревматоидный артрит, сопровождающийся увеличением селезенки и снижением количества лейкоцитов в крови (чаще нейтрофилов);
- болезнь Стилла у взрослых (эта форма ревматоидного артрита обычно развивается до 16 лет и имеет особые диагностические критерии).
Классификация DAS28 отражает степень активности ревматоидного артрита. Подсчет баллов осуществляется по специальной шкале, которая включает несколько пунктов:
- число опухших суставов;
- число болезненных суставов (учитывают 28 суставов: суставы запястья, пястно-фаланговые, проксимальные межфаланговые, локтевые, плечевые и коленные);
- уровень СОЭ или СРБ;
- общую оценку пациентом активности заболевания с помощью визуальной аналоговой шкалы (VAS/ВАШ, 0–100).
Симптомы ревматоидного артрита
Заболевание обычно начинается с полиартрита – воспаления нескольких суставов. Ревматоидный артрит часто развивается быстро, однако возможен так называемый продромальный период, который характеризуется у пациентов ощущением усталости, потерей массы тела, повышенной потливостью, «метеочувствительностью» суставов, небольшим подъемом температуры тела. Поражаются в основном суставы кистей рук и стоп, однако в некоторых случаях происходит поражение одного или нескольких крупных суставов (коленного, плечевого) с последующим вовлечением мелких суставов.
«Визитной карточкой» ревматоидного артрита является утренняя скованность – ощущение тугоподвижности суставов.
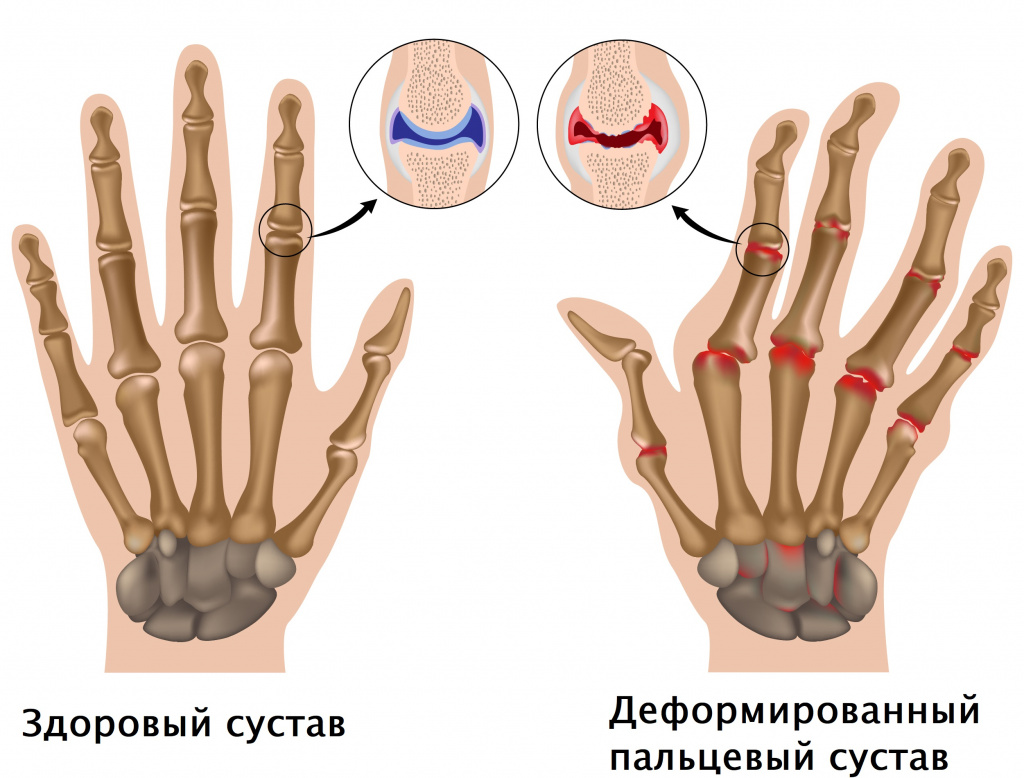
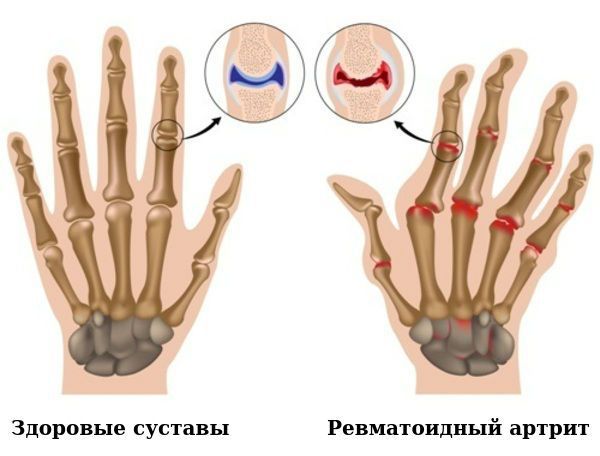
Появляется потребность размять пальцы для их нормального функционирования. Возможны и другие неприятные ощущения, мешающие активности пальцев рук. Прогрессирование заболевания порой приводит к полной неподвижности суставов в периоды обострения. Для ревматоидного артрита характерна симметричность поражения суставов. На ранней стадии заболевания происходит быстрое нарушение функциональной способности кистей рук, одним из симптомов которого является невозможность сжать кисть в кулак.
Пациенты с ревматоидным артритом в начале заболевания отмечают похудение кистей, что связано с атрофией мышц кисти (уменьшением мышечной массы).
Затем атрофия мышц может распространиться дальше — на плечи, бедра, голени.
При длительном течении активного воспалительного процесса формируются эрозии суставных поверхностей, происходят фиброзные изменения покровных тканей, нарушается их анатомическая целостность, развивается нестабильность суставов, что чревато их вывихами и подвывихами. Следующий этап — развитие контрактур (устойчивого ограничения движений в суставах), а в тяжелых случаях – их полная неподвижность.
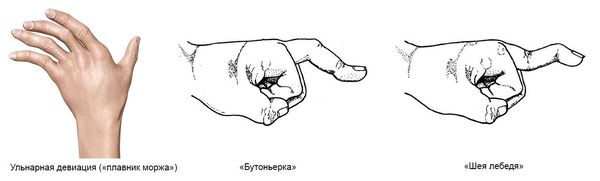
Типичный пример подвывиха — локтевая девиация кисти (отклонение пальцев в наружную сторону с формированием симптома «плавника моржа»). Возможна деформация пальцев по типу «шеи лебедя» – ближе к ладони палец постоянно согнут, а к концу – переразогнут
Среди внесуставных симптомов отмечаются ревматоидные узелки (до 30% больных). Они появляются на 3–5-м году заболевания и представляют собой округлые образования плотной консистенции, безболезненные, подвижные при ощупывании. Часто узелки располагаются в области локтей, крестца, волосистой части головы и на ахилловом сухожилии.
Диагностика ревматоидного артрита
Диагностика ревматоидного артрита проводится на основании жалоб пациента, данных осмотра и комплекса лабораторно-инструментальных методов обследования. Объем обследования может меняться в зависимости от клинической картины, тяжести заболевания, а также наличия осложнений.
- Клинический анализ крови: общий анализ с подсчетом тромбоцитов, лейкоформула, СОЭ (с микроскопией мазка крови при наличии патологических сдвигов).
С-реактивный белок (СРБ, CRP)
С-реактивный белок – белок острой фазы, чувствительный индикатор повреждения тканей при воспалении, некрозе, травме.
Синонимы: Анализ крови на СРБ; С-реактивн�…
Рентген костей кисти
Рентгенологическое исследование костей кисти предназначено для диагностики травматических повреждений, патологических изменений, а также оценки развития косте�…
Рентген костей стопы
Рентгенологическое исследование стопы в двух проекциях позволяет диагностировать травмы и другие патологические изменения, в том числе и плоскостопие.
К каким врачам обращаться
При появлении болей в суставах кистей рук, затруднении движений (как активных, так и пассивных), появлении утренней скованности суставов необходимо обратиться за консультацией к терапевту, педиатру, при подтверждении диагноза лечением заболевания будет заниматься ревматолог. Для проведения дифференциальной диагностики и определения тактики лечения может потребоваться консультация нефролога, невролога, кардиолога, пульмонолога.
Лечение ревматоидного артрита
Лечение ревматоидного артрита длительное и комплексное.
При выборе терапии врач опирается на множество факторов: давность заболевания, степень активности и выраженности процесса, тяжесть течения заболевания, наличие внесуставных проявлений и сопутствующих заболеваний.
Рекомендуется избегать интенсивных физических нагрузок, ограничить прием алкоголя и кофеина, отказаться от курения – все перечисленные факторы являются потенциальной причиной обострения заболевания и его более тяжелого течения. Необходимо контролировать массу тела для снижения нагрузки на суставы. Назначают сбалансированную диету, включающую полиненасыщенные жиры (оливковое масло, рыбий жир). Специалист по лечебной физкультуре подберет комплекс физических упражнений, полезных для суставов.
Важной частью лечения является медикаментозная терапия, которую назначает врач. В терапии используются следующие группы препаратов:
- нестероидные противовоспалительные средства для купирования активного воспаления и облегчения болевого синдрома;
- системные глюкокортикостероиды для контроля воспалительного процесса в суставах и усиления действия других препаратов;
- базисные противовоспалительные препараты эффективны при лечении ревматоидного артрита, но терапия должна проходить под контролем. Женщинам, принимающим данные препараты, необходимо использовать средства контрацепции и планировать беременность только после консультации с гинекологом;
- биологические препараты используют при неэффективности или непереносимости базисных препаратов.
В некоторых случаях может быть предложено хирургическое лечение.
Осложнения
Для ревматоидного артрита длительного течения характерно осложнение на почки. Амилоидоз или нефрит могут привести к полной дисфункции органа.
При развитии ревматоидного васкулита (поражения сосудов) наблюдаются длительно незаживающие раны и язвы, онемение конечностей, поражение сосудов легких, кишечника, почек с нарушением работы этих органов, появление кровоизлияний на коже.
Инфекционные осложнения развиваются на фоне снижения иммунитета при длительном применении препаратов, направленных на снижение иммунологической реактивности и замедление разрушения собственных тканей.
Профилактика ревматоидного артрита
Специфической профилактики не разработано.
Неспецифическая профилактика заключается в ведении здорового образа жизни, отказе от вредных привычек и умеренной физической нагрузке.
Источники:
- Клинические рекомендации «Ревматоидный артрит». Разраб.: Ассоциация ревматологов России, Российская ревматологическая ассоциация «Надежда». – 2021.
- Бокарев И.Н., Попова. И.Н. Внутренние болезни. Дифференциальная диагностика и лечение: Учебник. – М.: Издательство «Медицинское информационное агентство», 2015. 776 с.
- Хили П.М., Джекобсон Э. Дж. Дифференциальный диагноз внутренних болезней. Алгоритмический подход. Пер с англ. М.: Издательство «БИНОМ», 2014. 280 с.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет
Поделитесь этой статьей сейчас
Рекомендации
-
2937
02 Мая
-
5910
26 Апреля
-
5947
26 Апреля
Похожие статьи
Вросший ноготь
Вросший ноготь: причины появления, симптомы, диагностика и способы лечения.
Дерматомиозит
Дерматомиозит: причины появления, симптомы, диагностика и способы лечения.
Дата публикации 21 января 2020Обновлено 27 июня 2022
Определение болезни. Причины заболевания
Ревматоидный артрит — это хроническое воспалительное заболевание соединительной ткани, которое характеризуется повреждением суставов и системным поражением внутренних органов.
Краткое содержание статьи — в видео:
Чаще всего заболевание поражает именно суставы, но может также затрагивать другие системы (лёгкие, сердце и нервную систему). Повреждение суставов происходит вследствие хронического воспаления синовиальной оболочки — внутреннего слоя, выстилающего суставную сумку.
По мере прогрессирования болезни происходит эрозия кости и деформация суставов. Заболевание имеет аутоиммунный характер, это означает, что в организме образуются антитела против собственных тканей. В результате длительного воздействия этих антител происходит разрушение и воспаление тканей.
Распространённость в популяции взрослого населения составляет 0,5-2 % (у женщин < 65 лет ~ 5 %). Заболеваемость ревматоидным артритом составляет примерно 50-100 новых случаев на 100 000 населения в год [1]. Соотношение распространённости среди женщин и мужчин — 2-3:1. Поражаются все возрастные группы, включая детей и пожилых. Пик начала заболевания 30-55 лет.
Причины развития ревматоидного артрита неизвестны.
Предрасполагающие факторы:
- Инфекции (вирус Эпштейна — Барр, парвовирус В19 и др.).
- Генетические факторы, носительство антигена гистосовместимости HLA-DR4.
- Курение, злоупотребление кофе, высокий индекс массы тела, стресс.
- Контакт с минеральными маслами (моторными или гидравлическими). В эксперименте [13] было показано, что эти масла обладают артритогенными (т. е. вызывающими воспаление суставов) свойствами.
- Половые гормоны и факторы репродукции (беременность, роды и т. д.).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы ревматоидного артрита
В течении ревматоидного артрита выделяют продромальный период, который формируется за несколько недель и/или месяцев до развития типичного симптомокомплекса, присущего ревматоидному артриту. Он проявляется общей слабостью, недомоганием, болями в мышцах и суставах, снижением аппетита, субфебрильной температурой (от 37,1 до 38 °C) [1][2][8].
Дебют ревматоидного артрита может клинически проявляться различными вариантами:
- неспецифическими признаками с незначительно выраженным суставным проявлением (умеренные боли в суставах);
- острым полиартритом (боль, отёчность двух или трёх суставов, ограничение объёма движений в них) с преимущественным поражением суставов кистей, стоп, выраженной утренней скованностью;
- острым полиартритом с системными проявлениями: фебрильная лихорадка (температура от 38 до 39 °C); лимфаденопатия (увеличение лимфоузлов; могут увеличиться до размера грецкого ореха); гепатоспленомегалия (увеличение печени и селезёнки) [1].
Для ранней стадии РА характерно поражение второго и третьего проксимальных межфаланговых и пястно-фаланговых суставов, а также положительный симптом сжатия кисти или стопы (при сжатии кисти или стопы возникает резкая боль) на уровне пястно-фаланговых и плюснефаланговых суставов. Типичным симптомом РА является веретенообразная дефигурация (изменение формы сустава, например в виде лебединой шеи или пуговичной петли) проксимальных межфланговых суставов кистей.
Одним из наиболее ранних и характерных симптомов является утренняя скованность (пациент не может согнуть и разогнуть суставы, как будто руки в тугих перчатках). Выраженность скованности чётко взаимосвязана с воспалительной активностью. При высокой активности воспалительного процесса она длится на протяжении многих часов, однако по утрам особенно выражена и всегда снижается после двигательной активности.
В развёрнутой и финальной стадиях заболевания появляются типичные для РА деструкции, деформации и анкилозы (заращение сустава, отсутствие движений в нём).
Кисти:
- ульнарная девиация пястно-фаланговых суставов (пальцы отклоняются в локтевую сторону в виде плавников моржа), обычно через 1-5 лет от начала болезни;
- поражение пальцев кистей по типу «бутоньерки» (сгибание в проксимальном межфаланговом суставе) или «шеи лебедя» (переразгибание в проксимальном межфаланговом суставе);
- деформация кисти по типу «лорнетки» [1][5].
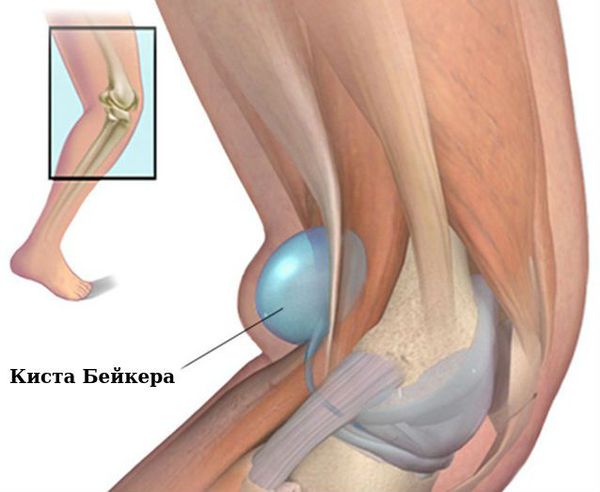
Коленные суставы: сгибательная и вальгусная (колени сводятся внутрь) деформация, киста Бейкера (подколенная или коленная киста).
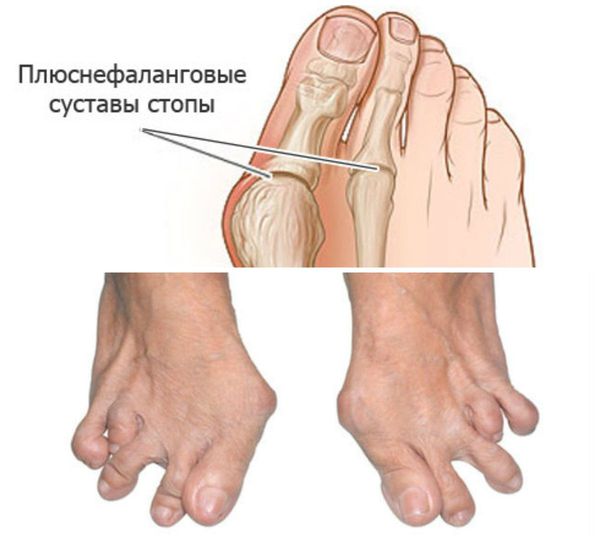
Стопы: подвывихи головок плюснефаланговых суставов, латеральная девиация (отклонение большого пальца к другим пальцам стопы), деформация большого пальца.
Шейный отдел позвоночника: подвывихи в области атлантоаксиального сустава, иногда осложняющиеся сдавлением спинного мозга или позвоночной артерии.
Перстневидно-черпаловидный сустав: огрубение голоса, одышка, дисфагия (пациент не может глотать), рецидивирующий бронхит.
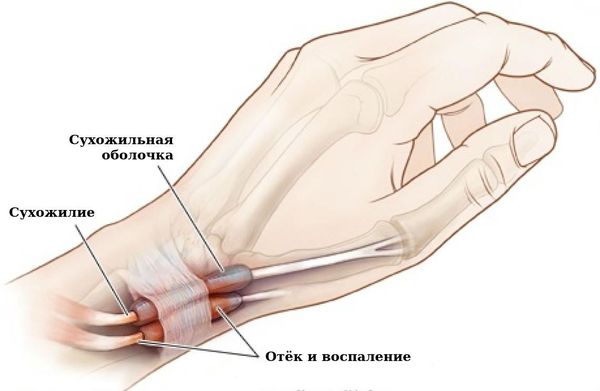
Связочный аппарат и синовиальные сумки: теносиновит (воспаление оболочек сухожилия) в области кисти и лучезапястного сустава; бурсит (воспаление в синовиальной сумке), чаще в области локтевого сустава; синовиальная киста на задней стороне коленного сустава (киста Бейкера).
Для РА характерны разнообразные внесуставные и системные проявления.
Конституциональные симптомы: генерализованная слабость, недомогание, похудение вплоть до истощения (вес меньше 40 кг), субфебрильная лихорадка.
В полиморфной картине ревматоидного артрита поражение сердца встречается нечасто. Кардиальная симптоматика может быть обусловлена как непосредственно воспалительным процессом в сердце, так и осложнением РА — атеросклерозом. При этом заболевании возможно вовлечение в патологический процесс миокарда (самой толстой мышцы сердца), перикарда (внешней оболочки сердца), эндокарда (внутренней оболочки сердца), аорты и венечных артерий сердца. Встречаются такие заболевания, как перикардит (воспаление внешней оболочки сердца), гранулематозное поражение клапанов сердца (очень редко), раннее развитие атеросклероза, воспаление коронарных артерий [1][6].
При РА нередко встречается поражение лёгких. Оно проявляется:
- плевритом (воспалением плевральных листков);
- интерстициальными поражениями лёгких (воспалением и нарушением структуры альвеолярных стенок, лёгочных капилляров);
- облитерирующим (обструктивным) бронхиолитом (стойкой, прогрессирующей закупоркой мелких бронхов);
- ревматоидными узелками в лёгких (синдром Каплана).
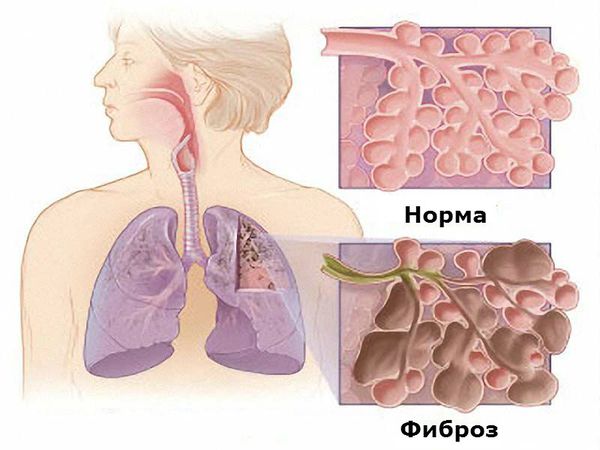
Наиболее серьёзным проявлением поражения лёгких является фиброзирующий альвеолит, который обусловлен как самим заболеванием, так и применением некоторых базисных противовоспалительных препаратов, а именно метотрексата, препаратов золота и Д-пеницилламина [1][6][7]. Фиброзирующий альвеолит проявляется непродуктивным кашлем (сухим, без мокроты), одышкой экспираторного типа (затруднён выдох), серым цианозом. Он приводит к повышению давления в лёгочной артерии и развитию лёгочного сердца (увеличению правых отделов сердца). На рентгенограмме определяется усиление лёгочного рисунка, феномен «медовых сот» (деструктивное изменение лёгких, характеризуется содержанием многочисленных кистозных воздушных пространств с толстыми стенками).
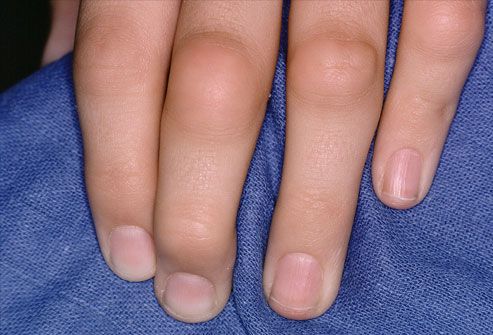
Кожный синдром имеет множество проявлений. Типичным внесуставным признаком являются ревматоидные узелки (костные образования на суставах размером с горошину или грецкий орех), которые располагаются под кожей чаще всего на разгибательной поверхности локтевых суставов, при атипичном расположении могут появляться на ахилловом сухожилии, роговице, в сухожилиях.
Кожными проявлениями ревматоидного артрита считают и развитие различных патологий:
- кожного васкулита (воспаления сосудов кожи) от язвенно-некротических изменений до утолщения и гипотрофии кожи;
- дигитального (пальцевого) артериита (воспаления и разрушения подкожных сосудов), редко с гангреной пальцев;
- микроинфарктов в области ногтевого ложа (нарушения кровообращения, закупорки сосуда микротромбом и появления чёрных точек на пальцах),
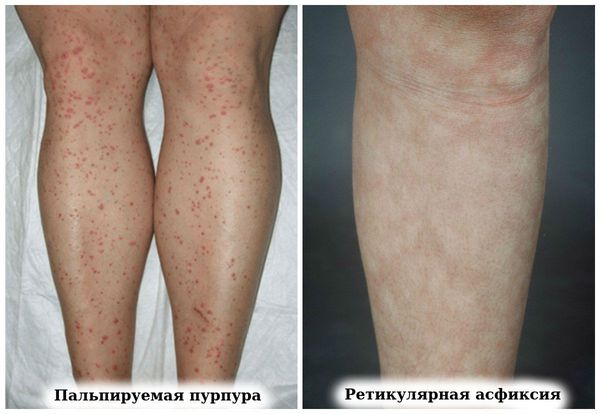
- сетчатого ливедо (ретикулярной асфиксии, или Livedo reticularis) — нежного рисунка синего цвета в виде кружева [8].
Поражения периферической нервной системы объясняются сдавлением нервных стволов или их сосудистым поражением. Для ревматоидного артрита характерны компрессионные нейропатии: синдром запястного канала (длительная боль, онемение пальцев кисти), тарзального канала (боль в области голеностопного сустава, чувство ползания мурашек по руке) и т. д. Компрессия нервных стволов проявляется болями, чувством ползания мурашек, онемением, регионарной атрофией мышц. Возможно и поражение периферических нервов, которое проявляется чувствительными или чувствительно-двигательными нарушениями.
Большое значение при ревматоидном артрите имеет поражение мышц: атрофия межкостных мышц кисти, тенора (возвышения большого пальца), гипотенора (возвышения мизинца). Характерна атрофия мышц, которые расположены близко к поражённым суставам, например атрофия межкостных мышц кистей, мышц нижней трети бедра в случае выраженного артрита коленных суставов. Амиотрофия (отсутствие мышц) может быть проявлением ревматоидного васкулита, нейропатии, например при синдроме запястного или локтевого канала, длительном применении глюкокортикоидов, ограничении мышечной активности [1][2][8].
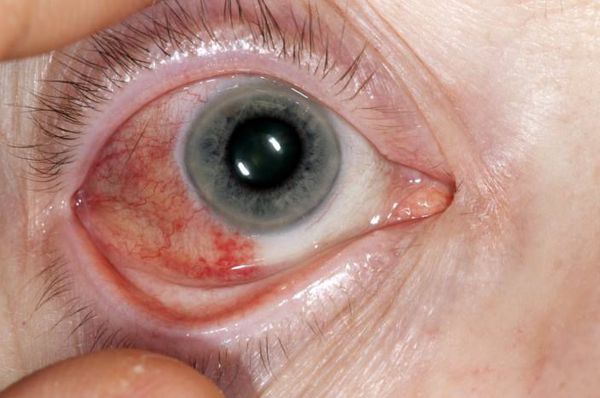
Патология глаз является одним из характерных проявлений ревматоидного артрита. Часто возникает эписклерит (воспаление тканей глаза), который очень редко сопровождается тяжёлым течением или исходом в перфорирующую склеромаляцию (размягчение ткани) с образованием отверстий в роговице и энуклеацией (удалением ядра).
При склерите (воспалении склеры глаза) и склерокератите (воспалении склеры и роговицы глаза) появляется выраженная боль и покраснение склеры. Характерен для этого заболевания и синдром сухого глаза, который является следствием скопления лимфоцитов в слёзных железах и обычно рассматривается в рамках синдрома Шегрена.
Патология почек проявляется диффузным гломерулонефритом (поражением клубочкового аппарата почек), распространённым амилоидозом (скоплением белка амилоида) с преимущественным поражением почек или лекарственной нефропатией (повреждением ткани и клубочкового аппарата почек). Последняя обусловлена приёмом нестероидных противовоспалительных средств (НПВС), например диклофенака, или комбинированных анальгетиков с фенацетином, что приводит к развитию интерстициального нефрита (воспаления в межуточной ткани почек).
Система крови реагирует на аутоиммунный воспалительный процесс развитием анемии, тромбоцитоза (увеличения содержания в крови тромбоцитов), нейтропении (снижения количества нейтрофилов). Возможны также вторичные, лекарственно обусловленные осложнения:
- в ответ на приём цитостатиков в виде панцитопении (снижения уровня всех видов кровяных клеток);
- на фоне высоких доз глюкокортикостероидов в виде лейкемоидной реакции (увеличения общего количества лейкоцитов).
Система макрофагов часто реагирует на активный воспалительный процесс развитием лимфаденопатии (увеличения лимфатических узлов), спленомегалии (увеличения селезёнки), формированием особой формы ревматоидного артрита в виде синдрома Фелти [2][7].
Поражение желудочно-кишечного тракта (ЖКТ) может быть представлено вторичным амилоидозом, аутоиммунным гепатитом, но наиболее часто выявляется эрозивное поражение вследствие приёма НПВС или глюкокортикостероидов.
У пациентов с высокой активностью ревматоидного артрита может развиваться васкулит:
- дигитальный артериит;
- пальпируемая пурпура (геморрагическая сыпь),
- ретикулярная асфиксия (пурпурный сетчатый сосудистый рисунок на коже);
- периферическая полинейропатия;
- висцеральный артериит: коронариит (воспалительное поражение стенок сосудов, питающих миокард), мезентериальный тромбоз (закупорка сосудов ткани, с помощью которой кишечник крепится к брюшной стенке), инфаркт кишечника, острый пневмонит, альвеолит);
- синдром Рейно (онемение и болевой синдром пальцев рук).
Эндокринные проявления — в связи с аутоиммунным характером заболевания одновременно могут развиваться аутоиммунный тиреоидит (хроническое заболевание щитовидной железы, при котором происходит постепенное разрушение клеток), синдром Шегрена.
Выделяют также редкие особые клинические формы течения ревматоидного артрита:
Синдром Фелти характеризуется таким симптомокомплексом: нейтропения, спленомегалия, гепатомегалия, тяжёлое поражение суставов, внесуставные проявления (васкулит, нейропатия, лёгочный фиброз, синдром Шегрена), гиперпигментация кожи нижних конечностей, высокий риск инфекционных осложнений. Этот синдром развивается у больных с длительным течением РА.
Болезнь Стилла у взрослых — рецидивирующая фебрильная лихорадка, артрит, макулопапулезная сыпь, высокая лабораторная активность. Он одинаково часто встречается у мужчин и женщин. Для этого синдрома характерна истощающая лихорадка, которая нередко достигает температуры выше 41 °C. Лихорадка носит стойкий характер и парадоксально реагирует на проводимую терапию. Поражение суставов характеризуется доброкачественным течением. При синдроме Стилла наблюдаются лейкоцитоз со сдвигом формулы влево, повышение активности печёночных ферментов, анемия, диспротеинемия (сдвиг белкового состава плазмы крови), ускоренная скорость оседания эритроцитов (СОЭ), повышение С-реактивного белка, который отражает острые воспалительные процессы в организме, гиперферритинемия (повышенный ферритин в крови) [1][8].
Патогенез ревматоидного артрита
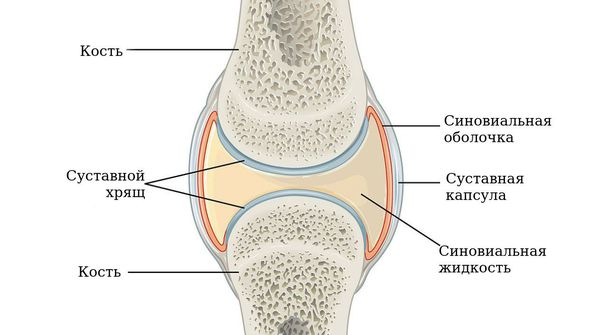
В норме синовиальная оболочка имеет толщину всего несколько клеток, она вырабатывает синовиальную жидкость, которая смазывает и питает сустав. Механизм развития ревматоидного артрита можно представить следующим образом.
- Ревматоидный артрит приводит к тому, что иммунные клетки атакуют здоровую синовиальную оболочку. Развивается субсиновиальный отёк, в синовиальной оболочке скапливаются лимфоциты, полиморфно-ядерные лейкоциты, моноциты и плазматические клетки.
- При этом иммунные клетки выделяют защитные белки — цитокины, которые провоцируют разрастание кровеносных сосудов синовиальной оболочки.
- Повышенный кровоток приводит к избыточному росту ткани. Синовиальные клетки быстро размножаются, что приводит к утолщению синовиальной ткани. Такая патологически утолщённая ткань называется «паннус».
- Клетки паннуса выделяют протеолитические ферменты, которые разрушают хрящ.
- Одновременно под воздействием гиперпродукции провоспалительных цитокинов (ФНО-альфа и др.) происходит активация остеокластов (клеток костной ткани, которые уничтожают старую структуру), что ведёт к повреждению костей. В дальнейшем происходит разрушение костной ткани с образованием эрозий.
- Костные эрозивные изменения происходят ещё и в результате активации фибробластов (главных клеток рыхлой соединительной ткани), которые начинают вырабатывать ферменты, способные разрушать суставной хрящ [1][2].
- Прогрессирование заболевания приводит к тому, что паннус превращается в зрелую фиброзную ткань, что ведёт к сращению суставных поверхностей.
Классификация и стадии развития ревматоидного артрита
Международная классификация болезней 10-го пересмотрм (МКБ-10):
- М05 — Серопозитивный ревматоидный артрит.
- М06 — Другие ревматоидные артриты.
- М05.0 — Синдром Фелти.
- М06.1 — Болезнь Стилла у взрослых.
- М06.9 — Ревматоидный артрит неуточнённый.
Рабочая классификация ревматоидного артрита (проект 2002):
Серопозитивный ревматоидный артрит (М 05).
- Полиартрит (М05).
- Ревматоидный васкулит (М 05.2) (дигитальный артериит, хронические язвы кожи, синдром Рейно и др.).
- Ревматоидные узлы (М 05.3).
- Полинейропатия (М 05.3).
- Ревматоидная болезнь лёгких (М 05.1) (альвеолит, ревматоидные лёгкие).
- Синдром Фелти (М 05.1).
Серонегативный ревматоидный артрит (М 06.0).
- Полиартрит (М 06.0).
- Синдром Стилла взрослых (М 06.1) [14].
В течение длительного времени для установления достоверного диагноза РА использовались критерии 1987 года.
Пересмотренные диагностические критерии РА (ARA 1987):
- Утренняя скованность (не менее 1 часа).
- Артрит трёх или более суставных зон.
- Артрит суставов кистей.
- Симметричный артрит.
- Ревматоидные узелки.
- Ревматоидный фактор.
- Рентгенологические изменения.
Достоверный диагноз РА устанавливают при наличии четырёх из семи вышеперечисленных критериев, причём первые четыре должны существовать не менее шести недель.
В настоящее время доказана возможность изменения отрицательного прогноза РА в случае раннего начала патогенетической базисной терапии. Поэтому длительное время разрабатывались методы ранней диагностики РА. В 2010 году ассоциацией американских и европейских ревматологов были приняты критерии ранней диагностики РА, в которых клинические и лабораторные показатели выражены в баллах. При суммарной величине более 6 баллов может быть установлен достоверный диагноз ранней стадии РА, что предполагает возможность начала патогенетической терапии базисными препаратами [1][2][6].
| А. Поражение суставов | Баллы |
|---|---|
| 1 большой сустав | 0 |
| 2-10 больших суставов | 1 |
| 1-3 малых суставов | 2 |
| 4-10 малых суставов | 3 |
| Больше 10 суставов | 4 |
| В. Серологический тест | |
| Отрицательные РФ АЦП | 0 |
| Слабо + тесты на РФ и АЦП | 1 |
| Высоко + тесты на РФ и АЦП | 2 |
| С. Маркеры острой фазы воспаления | |
| Нормальный СРБ и СОЭ | 0 |
| Аномальные СОЭ и СРБ | 1 |
| D. Длительность симптомов | |
| Меньше 6 недель | 0 |
| Больше 6 недель | 1 |
Наличие 6 из 10 баллов указывает на определённый РА.
В 2007 году Ассоциации ревматологов России приняла новую классификацию РА, включающую несколько разделов.
Основной диагноз:
- Ревматоидный артрит серопозитивный (М05.8).
- Ревматоидный артрит серонегативный (М06.0).
- Особые клинические формы ревматоидного артрита:
- синдром Фелти (М05.0);
- болезнь Стилла, развившаяся у взрослых (М06.1).
- Ревматоидный артрит вероятный (М05.9, М06.4, М06.9).
Клиническая стадия:
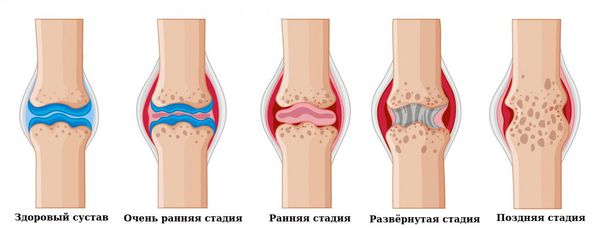
- Очень ранняя стадия: длится меньше 6 месяцев.
- Ранняя стадия: длится от 6 месяцев до года.
- Развёрнутая стадия: длится больше года при наличии типичной симптоматики ревматоидного артрита.
- Поздняя стадия: длится 2 года и более, протекает с выраженным повреждением мелких (III-IV рентгенологическая стадия) и крупных суставов, наличие осложнений.
Активность болезни:
- 0 = ремиссия: DAS28 < 2,6 (DAS28 — индекс активности болезни).
- 1 = низкая: 2,6 < DAS28 <3,2.
- 2 = средняя: DAS28 = 3,2-5,1.
- 3 = высокая (DAS28 > 5,1).
Внесуставные (системные) проявления:
- Ревматоидные узелки.
- Кожный васкулит (язвенно-некротический васкулит, инфаркты ногтевого ложа, дигитальный артериит, ливедо-ангиит).
- Васкулит других органов.
- Нейропатия (мононеврит, полинейропатия).
- Плеврит (сухой, выпотной), перикардит (сухой, выпотной).
- Синдром Шегрена.
- Поражение глаз (склерит, эписклерит, васкулит сетчатки).
Инструментальная характеристика:
- Наличие эрозий (с использованием рентгенографии, возможно МРТ, УЗИ):
- неэрозивный;
- эрозивный.
- Рентгенологическая стадия (по Штейнброкеру, модификация):
- I — околосуставной остеопороз.
- II — остеопороз + сужение суставной щели, возможны единичные эрозии.
- III — признаки предыдущей стадии + множественные эрозии + подвывихи в суставах.
- IV — признаки предыдущей стадии + костный анкилоз.
Дополнительная иммунологическая характеристика — антитела к циклическому цитрулинированному пептиду (АЦЦП). Цитруллинированный пептид — это белок, который вырабатывается в результате обменных процессов в организме. В норме цитруллин полностью выводится из организма. При развитии РА концентрация ЦЦП повышается, иммунная система воспринимает его как чужеродный и начинает вырабатывать к нему антитела.
- АЦЦП — присутствуют (+);
- АЦЦП — отсутствуют (-).
Функциональный класс:
- I — пациент выполняет все три жизненно-важные функции: самообслуживание, профессиональные и непрофессиональные обязанности.
- II — пациент ограничен только в непрофессиональной деятельности (все элементы досуга, отдых, развлечения, занятия спортом).
- III — ограничена непрофессиональная и профессиональная деятельность (работа и учёба, ведение домашнего хозяйства), но сохранена возможность самообслуживания.
- V — утрачены все три жизненно-важные функции, даже возможность самообслуживания [14].
Осложнения ревматоидного артрита
- Амилоидоз почек возможен при длительном течении ревматоидного артрита. Проявляется отёками, повышением артериального давления, большим количеством белка в анализах мочи. Т. е. за сутки теряется 3-20 г белка. Диагноз может быть подтверждён биопсией почки.
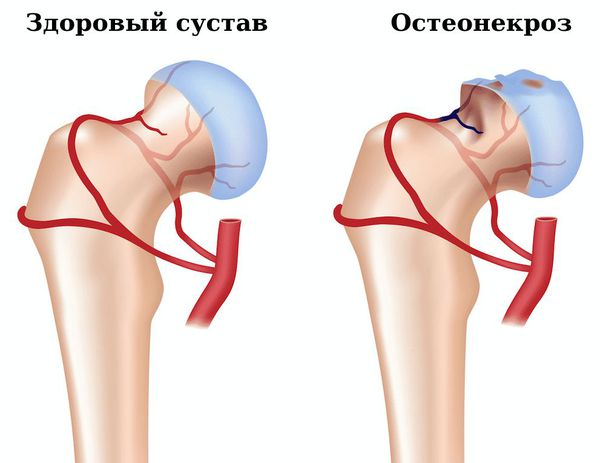
- Остеонекроз — омертвение участка кости, вызванное нарушением кровоснабжения. Появляется сильная боль в поражённом суставе, ограничение объёма движений в нём. Для подтверждения диагноза необходимо сделать рентгенографию, компьютерную томографию сустава.
- Вторичный остеоартроз — появление болей в суставе, хруст при движении в нём, может быть отёчность. Для подтверждения диагноза надо сделать рентген сустава.
- Туннельные синдромы — неврологическое заболевание, проявляющиеся длительной болью и онемением пальцев кисти. Причиной заболевания является сдавление срединного нерва между костями, поперечной кистевой связкой и сухожилиями мышц запястья.
- Кардиоваскулярные проявления — для пациентов с ревматоидным артритом характерно раннее развитие атеросклероза. Поэтому возможно возникновения инсульта и инфаркта [12].
- Медикаментозные ятрогении (токсические и аллергические) — это патологические состояния, вызванные медицинским вмешательством. Т. е. под влиянием медицинских воздействий могут возникнуть новые заболевания у пациента, либо осложнение, либо ухудшение уже имеющегося заболевания.
Также к осложнениям относятся рак желудочно-кишечного тракта, остеопороз, синдром Сикки, синдром Фелти, лимфома и др. [12].
Диагностика ревматоидного артрита
Лабораторные исследования, рекомендуемые для обследования пациентов с подозрением на ревматоидный артрит [2]:
- Общий анализ крови с подсчётом количества тромбоцитов.
- Биохимический анализ крови (общий белок, альбумин, глобулиновые фракции, общий билирубин, мочевина, креатинин, электролиты, кальций, холестерин, липидный спектр крови, С-реактивный белок, ревматоидный фактор).
- Исследование уровня антител к циклическому цитруллинированному пептиду (АЦЦП).
- Общий анализ мочи, определение белка в моче.
- Исследование сывороточных иммуноглобулинов
Ранняя диагностика подразумевает исследование уровня АЦЦП:
- АЦЦП — обязательно выполняется для ранней диагностики ревматоидного артрита, т. к. является более чувствительным и специфичным серологическим маркером раннего ревматоидного артрита, чем ревматоидный фактор (РФ). (РФ — белки, которые вырабатываются иммунной системой человека и атакуют собственные клетки, ошибочно воспринимая их как чужеродные.)
- АЦЦП выявляются у 40-50 % больных ревматоидным артритом с отрицательным РФ.
- АЦЦП «+» является показанием к началу антиревматической терапии на ранней стадии (менее шести месяцев), что позволяет эффективно затормозить прогрессирующее поражение суставов.
- АЦЦП «+» значимо для дифференциальной диагностики и прогнозирования течения ревматоидного артрита.
Инструментальные методы диагностики, рекомендуемые для обследования пациентов с подозрением на ревматоидный артрит:
- рентгенография суставов;
- УЗИ суставов;
- МРТ суставов;
- артроскопия;
- диагностическая пункция сустава: иммунологическое, цитологическое исследование, бактериальный посев синовиальной жидкости.
Дифференциальный диагноз следует проводить со следующими заболеваниями: остеоартроз, системная красная волчанка, подагра, псориатический артрит, анкилозирующий спондилит, реактивный артрит, бактериальный эндокардит, септический артрит, вирусные артриты, системная склеродермия, идиопатические воспалительные миопатии, смешанное заболевание соединительной ткани, болезнь Лайма, амилоидоз, саркоидоз, рецидивирующий полихондрит, фибромиалгия.
Лечение ревматоидного артрита
Цели: уменьшение или устранение симптомов артрита и внесуставных проявлений, контроль над воспалительной активностью, предотвращение прогрессирования костно-суставной деструкции, сохранение и существенное улучшение качества жизни, увеличение продолжительности жизни до среднего уровня в популяции [3][5][10].
Treat to Target (T2T) — лечение до достижения цели (рекомендации EULAR)
Общие рекомендации:
- Исключение стрессов.
- Исключение чрезмерного облучения солнечной радиацией. Интенсивное солнце тоже провоцирует развитие ревматических заболеваний.
- Активное лечение сопутствующих инфекций, при необходимости вакцинация.
- Профилактика атеросклероза: употребление пищи с малым содержанием жира, холестерина и высоким содержанием полиненасыщенных жирных кислот, отказ от курения, контроль массы тела, физические упражнения, приём фолиевой кислоты.
- Профилактика остеопороза: пища с высоким содержанием кальция, приём витамина Д, возможно назначение бисфосфонатов.
Медикаментозное лечение
Базисная терапия ревматоидного артрита
БПВП — базисные противовоспалительные препараты (синонимы: базисные препараты, болезнь-модифицирующие антиревматические препараты, медленно действующие препараты) — главный компонент лечения РА, при отсутствии противопоказаний они должны быть назначены каждому пациенту с этим диагнозом. Особенно важно назначение БПВП сразу после установления диагноза на ранней стадии, когда имеется ограниченный период времени (несколько месяцев) для достижения наилучших отдалённых результатов — так называемое «терапевтическое окно» [9][10].
Метотрексат — один из основных препаратов терапии РА. Цитотоксический препарат из группы антиметаболитов. По структуре аналог фолиевой кислоты. Каждому пациенту с РА при отсутствии явных противопоказаний должна быть назначена терапия метотрексатом.
Метотрексат является препаратом выбора при активном ревматоидном артрите, как на ранней, так и в развёрнутой и поздней стадиях. Этот препарат обладает значительной терапевтической широтой и возможностью индивидуального подбора дозировок, эффективные дозы находятся в диапазоне 15-30 мг/нед, в среднем — 20 мг/нед.
Метотрексат достаточно безопасен, требует минимального лабораторного контроля (общий анализ крови и трансаминазы), целесообразно назначение фолиевой кислоты 3-5 мг/сут в дни без введения препарата [5][11]. Применяют внутрь, подкожно и внутримышечно.
Основные нежелательные явления: М-эрозивный стоматит, эрозивный гастрит, диспепсия, геморрагический энтероколит, гепатоцеллюлярный синдром, нефротоксичность, обструктивная мочекислая нефропатия.
Лефлуномид («Арава») — антивоспалительное, иммуномодулирующее, антипролиферативное действие. Специально был разработан для лечения РА.
Нежелательные явления: желудочно-кишечная токсичность, печёночная токсичность, кожная сыпь, алопеция, цитопении, фиброзирующий альвеолит, снижение веса, лихорадка, почечная токсичность — при их развитии необходим приём холестирамина по 8 г три раза в день в течение 11 дней [5][10][11].
Биологическая терапия РА
Введение ГИБП (генно-инженерных биологических препаратов) стало главным прорывом в лечении ревматических заболеваний. ГИПБ представляют собой искусственные антитела (белки из группы иммуноглобулинов). С появлением биологических препаратов появилась возможность достичь длительной и стойкой ремиссии у больных с ревматоидным артритом. В настоящее время ГИБП разделены на группы по их механизму действия:
- препараты, направленные на подавление продукции ФНО-альфа (фактора некроза опухоли): инфликсимаб, этанерцепт, адалимумаб, цертолизумаб пегол, голимумаб [1][5][8].
- ингибиторы иммуноглобулинов: ИЛ-1, ИЛ-6.
- абатацепт — растворимый белок, направленный на подавление ко-стимуляции Т-клеток,
- препараты, блокирующие действие В-клеток (ритуксимаб и белимумаб), применяются при ревматоидном артрите и системной красной волчанке.
В последнее время в лечении серонегативных спондилоартритов, включая псориатический артрит, широко используются устекинумаб (блокатор ИЛ-1223) и секукинумаб (ингибитор ИЛ-17) [8][9].
Побочные эффекты. Биологические препараты помимо положительных свойств обладают и отрицательными:
- Снижение противоинфекционного и (потенциально) противоопухолевого иммунитета. Общими для всех антагонистов ФНО-альфа нежелательными побочными реакциями (НПР) является повышение восприимчивости к инфекциям, включая возможность обострения гистоплазмоза (грибкового заболевания) и гепатита В. Появляется риск развития демиенилизирующих заболеваний, волчаночноподобного синдрома (лекарственной волчанки, которая возникает в результате приёма медикаментозных препаратов), злокачественных новообразований, тромбоэмболии (закупорки кровеносного сосуда тромбом), реакции гиперчувствительности. Среди наиболее частых НПР фигурируют назофарингит (воспаление слизистой оболочки носоглотки), инфекции мочевых и верхних дыхательных путей, боль в животе, диарея, появление АНФ (антинуклеарного фактора, который показывает наличие или отсутствие аутоиммунного заболевания) и антител к двуспиральной ДНК. Особенно возрастает восприимчивость организма к туберкулёзу. При применении антагонистов ФНО-альфа туберкулёз может давать атипичную клиническую картину. Учитывая это, до начала терапии ГИБП все пациенты должны быть обследованы на предмет как активной так и латентной туберкулёзной инфекции: проба Манту, Диаскин-тест [3][6].
- Риск развития аллергических реакций и иммуногенность, т. е. реакция собственной иммунной системы на ГИБП, которые содержат чужеродный мышиный белок. Вырабатываемые при этом нейтрализующие антитела к ГИБП снижают эффективность проводимой терапии и способствуют развитию инфузионныхпостинъекционных реакций. Чаще всего эти антитела образуются к инфликсимабу, содержащему больше мышиного компонента, чем гуманизированные анти-ФНО-альфа препараты. Частота их появления при РА составляет от 7 до 53 % в зависимости от дозы. Назначение инфликсимаба в комбинации с метотрексатом снижает вероятность образования антител. При лечении этанерцептом и адалимумабоб антитела выявляются реже (5-17 %). При применении адалимумаба в комбинациии с метотрексатом частота возникновения антител минимальна и составляет около 1 % [1][4][6].
Действие антагонистов ФНО альфа вызывает небольшое, но длительно сохраняющееся увеличение содержания холестерина ЛПВП (так называемый «хороший» холестерин). Которое, в свою очередь, может оказать благоприятный эффект на сердечно-сосудистые риски у пациентов с хроническим артритом. Доказано снижение частоты сердечно-сосудистой патологии и летальности в группе больных РА, получавших лечение анти-ФНО-альфа препаратами, по сравнению с пациентами, в комплексной терапии которых данная группа препаратов не использовалась. С другой стороны, следует иметь в виду, что у больных РА с застойной сердечной недостаточностью антагонисты ФНО-альфа должны применяться с особой осторожностью. Поскольку они способны приводить к декомпенсации кровообращения и увеличению летальности. Выраженная хроническая сердечная недостаточность является противопоказанием для назначения ГИБП [4][9].
Класс малых молекул
Тофацитиниб («Яквинус») — препарат нового класса для терапии РА. Он может использоваться как в качестве монотерапии, так и в сочетании с метотрексатом или другими БПВП вне зависимости от приёма пищи [4][6].
Симптоматическая терапия
НПВП — нестероидные противовоспалительные препараты. Их особенность — быстрое наступление терапевтического эффекта, активное подавление боли и воспаления (диклофенак, «Нимесил», «Найз», «Аркоксия» и др.)
ГКС — глюкокортикостероиды. Применяются в следующих случаях:
- при максимальной активности воспалительного процесса;
- при интенсивных болях, не купирующихся НПВП;
- при генерализованном артрите с экссудативными проявлениями;
- при системных проявлениях РА;
- как компонент bridge-терапии («Метипред», преднизолон, «Полькортолон»)
Локальная терапия ГКС — внутрисуставно и периартикулярно: бетаметазона дипропионат-дипроспан; триамцинолона ацетонид («Кеналог»); гидрокортизон ацетат.
Немедикаментозное лечение
Несмотря на то, что медикаментозная терапия является главным компонентом лечения РА, немедикаментозные методы играют важную роль в достижении полноценного лечебного эффекта. Цель реабилитационных мероприятий — восстановление нарушенных или утраченных способностей пациента, его адаптация к хроническому заболеванию [3].
Лечебная физкультура и трудотерапия (специальные упражнения, имитирующие движения в процессе самообслуживания, направленные на восстановление моторики) полезны больным РА.
Физиотерапия и бальнеотерапия полезны пациентам с низкой активностью воспаления, они могут заметно уменьшить симптоматику и улучшить подвижность [3].
Прогноз. Профилактика
Прогноз
Показатели смертности у больных РА увеличиваются: средняя продолжительность жизни снижается на 8-15 лет. Около 40 % пациентов в течение трёх лет становятся нетрудоспособными. Примерно у 80 % в течение 20 лет развивается нетрудоспособность средней и тяжёлой степени и в 25 % случаев требуется обширное протезирование суставов.
Факторы неблагоприятного прогноза: женский пол, положительный РФ, поражение плюснефаланговых суставов в начале заболевания.
РА является дорогостоящим заболеванием. Это связано как со стоимостью медицинских расходов, так и со снижением работоспособности больного вплоть до её полной потери. Особенно высоки прямые и непрямые затраты при неэффективности лечения [5][7]. Однако современные методы лечения, особенно комбинированная терапия активными синтетическими и биологическими противовоспалительными препаратами, могут снизить краткосрочные и долгосрочные затраты на лечение тяжёлого РА. Эти данные следует учитывать при рассмотрении плана лечения конкретного больного.
Профилактика
Этиология РА неизвестна, первичная профилактика не проводится [1]. Скрининг не проводится.
Ревматоидный артрит — тяжёлое заболевание, которое меняет жизнь человека. Многие пациенты впадают в отчаяние и думают, что так тяжело будет всегда. Но это не так. Важно лечиться, выполнять назначения врача, не бояться информации о своей болезни. Нужно уметь расслабляться, соблюдать режим, не стесняться делиться своими эмоциями, страхами, переживаниями, наблюдениями. Нужно всегда помнить, что душевное равновесие, внутреннее спокойствие и позитивный настрой — лучшие союзники в борьбе с болезнью [3].
Важно иметь в виду, что предварительные результаты свидетельствуют о выявлении иммунологических нарушений (увеличение титров РФ, анти-ЦБ, и СРБ) за несколько месяцев или лет до появления клинических симптомов РА [1].
Ревматоидный артрит — это заболевание, находящееся в фокусе внимания ревматологов всего мира в течение десятилетий. Это связано с большим медицинским и социальным значением этой болезни. Ее распространенность достигает 0,5–2% от общей численности населения в промышленно развитых странах [1, 2]. У больных ревматоидным артритом наблюдается уменьшение продолжительности жизни по сравнению с общей популяцией на 3–7 лет [3]. Трудно переоценить колоссальный ущерб, наносимый этим заболеванием обществу за счет ранней инвалидизации пациентов, которая при отсутствии своевременно начатой активной терапии может наступать в первые 5 лет от дебюта болезни.
Ревматоидный артрит — хроническое воспалительное заболевание неясной этиологии, для которого характерно поражение периферических синовиальных суставов и периартикулярных тканей, сопровождающееся аутоиммунными нарушениями и способное приводить к деструкции суставного хряща и кости, а также к системным воспалительным изменениям.
Патогенез заболевания весьма сложен и во многом недостаточно изучен. Несмотря на это, к настоящему времени хорошо известны некоторые ключевые моменты в развитии ревматоидного воспаления, которые определяют основные методы лечебного воздействия на него (рис. 1). Развитие хронического воспаления в данном случае связано с активацией и пролиферацией иммунокомпетентных клеток (макрофагов, Т- и В-лимфоцитов), что сопровождается выделением клеточных медиаторов — цитокинов, факторов роста, молекул адгезии, а также синтезом аутоантител (например, антицитруллиновых антител) и формированием иммунных комплексов (ревматоидные факторы). Эти процессы ведут к формированию новых капиллярных сосудов (ангиогенез) и разрастанию соединительной ткани в синовиальной оболочке, к активации циклооксигеназы-2 (ЦОГ-2) с повышением синтеза простагландинов и развитием воспалительной реакции, к выделению протеолитических ферментов, активации остеокластов, а в результате — к деструкции нормальных тканей суставов и возникновению деформаций.
Лечение ревматоидного артрита
Лечение включает:
- медикаментозную терапию;
- немедикаментозные методы терапии;
- ортопедическое лечение, реабилитацию.
Исходя из патогенеза заболевания, становится очевидным, что эффективно воздействовать на развитие заболевания можно на двух уровнях:
- подавляя избыточную активность иммунной системы;
- блокируя выработку медиаторов воспаления, в первую очередь простагландинов.
Поскольку, помимо собственно воспаления, активация иммунной системы сопровождается многими другими патологическими процессами, воздействие на первом уровне является существенно более глубоким и эффективным, нежели на втором. Медикаментозная иммуносупрессия представляет собой основу лечения ревматоидного артрита. К иммуносупрессорам, применяющимся для лечения данного заболевания, относятся базисные противовоспалительные препараты (БПВП), биологические препараты и глюкокортикостероиды. На втором уровне действуют нестероидные противовоспалительные препараты (НПВП) и глюкокортикостероиды.
В целом иммуносупрессивная терапия сопровождается более медленным развитием клинического эффекта (в широких рамках — от нескольких дней в случае биологической терапии до нескольких месяцев в случае применения некоторых БПВП), который в то же время бывает очень выраженным (вплоть до развития клинической ремиссии) и стойким, а также характеризуется торможением деструкции суставов.
Собственно противовоспалительная терапия (НПВП) может давать клинический эффект (обезболивание, уменьшение скованности) очень быстро — в течение 1–2 ч, однако при помощи такого лечения практически невозможно полностью купировать симптоматику при активном ревматоидном артрите и, по-видимому, оно совсем не влияет на развитие деструктивных процессов в тканях.
Глюкокортикостероиды обладают как иммуносупрессивным, так и непосредственным противовоспалительным эффектом, поэтому клиническое улучшение может развиваться быстро (в течение нескольких часов при внутривенном или внутрисуставном введении). Имеются данные о подавлении прогрессирования эрозивного процесса в суставах при длительной терапии низкими дозами глюкокортикостероидов и о положительном их влиянии на функциональный статус больного. В то же время из практики хорошо известно, что назначение только глюкокортикостероидов, без других иммуносупрессивных средств (БПВП), редко дает возможность достаточно эффективно контролировать течение болезни.
Немедикаментозные способы терапии ревматоидного артрита (физиотерапия, бальнеотерапия, диетотерапия, акупунктура и др.) представляют собой дополнительные методики, с помощью которых можно несколько улучшить самочувствие и функциональный статус пациента, но не купировать симптоматику и достоверно повлиять на деструкцию суставов.
Ортопедическое лечение, включающее ортезирование и хирургическую коррекцию деформаций суставов, а также реабилитационные мероприятия (лечебная физкультура и др.) имеют особое значение преимущественно на поздних стадиях заболевания для поддержания функциональной способности и улучшения качества жизни больного.
Основными целями лечения при РА являются [2, 6]:
- купирование симптомов заболевания, достижение клинической ремиссии или как минимум низкой активности болезни;
- торможение прогрессирования структурных изменений в суставах и соответствующих функциональных нарушений;
- улучшение качества жизни больных, сохранение трудоспособности.
Надо иметь в виду, что цели лечения могут существенно изменяться в зависимости от длительности болезни. На ранней стадии болезни, т. е. при длительности болезни 6–12 мес, достижение клинической ремиссии — вполне реальная задача, так же как и торможение развития эрозий в суставах. С помощью современных методов активной медикаментозной терапии удается добиться ремиссии у 40–50% пациентов [4, 5], показано также отсутствие появления новых эрозий по данным рентгенографии [7] и магнитно-резонансной томографии [8] у значительного количества больных при длительности наблюдения 1–2 года.
При длительно текущем ревматоидном артрите, особенно при недостаточно активной терапии в первые годы заболевания, достижение полной ремиссии теоретически тоже возможно, однако вероятность этого значительно ниже. То же самое можно сказать и о возможности остановить прогрессирование деструкции в суставах, уже существенно разрушенных за несколько лет болезни. Поэтому при далеко зашедшем ревматоидном артрите возрастает роль реабилитационных мероприятий, ортопедической хирургии. Кроме того, на поздних стадиях заболевания длительная поддерживающая базисная терапия может использоваться для вторичной профилактики осложнений болезни, таких как системные проявления (васкулит и др.), вторичный амилоидоз.
Базисная терапия ревматоидного артрита. БПВП (синонимы: базисные препараты, болезнь-модифицирующие антиревматические препараты, медленно действующие препараты) являются главным компонентом лечения ревматоидного артрита и при отсутствии противопоказаний должны быть назначены каждому пациенту с этим диагнозом [9]. Особенно важно максимально быстрое назначение БПВП (сразу после установления диагноза) на ранней стадии, когда имеется ограниченный период времени (несколько месяцев от появления симптоматики) для достижения наилучших отдаленных результатов — так называемое «терапевтическое окно» [10].
Классические БПВП обладают следующими свойствами.
- Способность подавлять активность и пролиферацию иммунокомпетентных клеток (иммуносупрессия), а также пролиферацию синовиоцитов и фибробластов, что сопровождается выраженным снижением клинико-лабораторной активности РА.
- Стойкость клинического эффекта, в том числе его сохранение после отмены препарата.
- Способность задерживать развитие эрозивного процесса в суставах.
- Способность индуцировать клиническую ремиссию.
- Медленное развитие клинически значимого эффекта (обычно в течение 1–3 мес от начала лечения).
БПВП существенно различаются между собой по механизму действия и особенностям применения. Основные параметры, характеризующие БПВП, представлены в таблице 1.
БПВП условно могут быть подразделены на препараты первого и второго ряда. Препараты первого ряда обладают наилучшим соотношением эффективности (достоверно подавляют как клиническую симптоматику, так и прогрессирование эрозивного процесса в суставах) и переносимости, в связи с чем назначаются большинству пациентов.
К БПВП первого ряда относятся следующие.
- Метотрексат — «золотой стандарт» терапии ревматоидного артрита. Рекомендуемые дозы — 7,5–25 мг в неделю — подбираются индивидуально путем постепенного повышения на 2,5 мг каждые 2–4 нед до достижения хорошего клинического ответа либо возникновения непереносимости. Препарат дается внутрь (еженедельно в течение двух последовательных дней дробно в 3–4 приема каждые 12 ч). В случае неудовлетворительной переносимости метотрексата при приеме внутрь за счет диспепсии и других жалоб, связанных с желудочно-кишечным трактом (ЖКТ), препарат может быть назначен парентерально (одна в/м или в/в инъекция в неделю).
- Лефлуномид (арава). Стандартная схема лечения: внутрь по 100 мг в сутки в течение 3 дней, затем 20 мг/сут постоянно. При риске непереносимости препарата (пожилой возраст, заболевания печени и др.) лечение можно начинать с дозы 20 мг/сут. По эффективности сопоставим с метотрексатом, имеет несколько лучшую переносимость. Есть данные о более высокой эффективности лефлуномида в отношении качества жизни больных, особенно при раннем ревматоидном артрите. Стоимость лечения лефлуномидом достаточно высока, поэтому он чаще назначается при наличии противопоказаний к применению метотрексата, его неэффективности или непереносимости, однако может использоваться и как первый базисный препарат.
- Сульфасалазин. В клинических испытаниях не уступал по эффективности другим БПВП, однако клиническая практика показывает, что достаточный контроль над течением болезни сульфасалазин обычно обеспечивает при умеренной и низкой активности ревматоидного артрита.
БПВП второго ряда применяются значительно реже в связи с меньшей клинической эффективностью и/или большей токсичностью. Они назначаются, как правило, при неэффективности или непереносимости БПВП первого ряда.
БПВП способны вызвать значительное улучшение (хороший клинический ответ) приблизительно у 60% пациентов. В связи с медленным развитием клинического эффекта назначение БПВП на сроки менее 6 мес не рекомендуется. Длительность лечения определяется индивидуально, типичная продолжительность «курса» лечения одним препаратом (в случае удовлетворительного ответа на терапию) составляет 2–3 года и более. Большинство клинических рекомендаций подразумевают неопределенно долгое применение поддерживающих дозировок БПВП для сохранения достигнутого улучшения.
При недостаточной эффективности монотерапии каким-либо базисным препаратом может быть избрана схема комбинированной базисной терапии, т. е. сочетания двух-трех БПВП. Наиболее хорошо зарекомендовали себя следующие сочетания:
- метотрексат + лефлуномид;
- метотрексат + циклоспорин;
- метотрексат + сульфасалазин;
- метотрексат + сульфасалазин + гидроксихлорохин.
В комбинированных схемах препараты обычно применяются в средних дозировках. В ряде клинических исследований было продемонстрировано превосходство комбинированной базисной терапии над монотерапией, однако более высокая эффективность комбинированных схем не считается строго доказанной. Комбинация БПВП ассоциирована с умеренным повышением частоты побочных эффектов.
Биологические препараты в лечении ревматоидного артрита. Термин биологические препараты (от англ. biologics) применяется по отношению к лекарственным средствам, производимым с использованием биотехнологий и осуществляющим целенаправленное («точечное») блокирование ключевых моментов воспаления с помощью антител или растворимых рецепторов к цитокинам, а также другим биологически активным молекулам. Таким образом, биологические препараты не имеют никакого отношения к «биологически активным пищевым добавкам». В связи с большим количеством «молекул-мишеней», воздействие на которые потенциально может подавлять иммунное воспаление, разработан целый ряд лекарственных средств из этой группы и еще несколько препаратов проходят клинические испытания.
К основным зарегистрированным в мире для лечения ревматоидного артрита биологическим препаратам относятся:
- инфликсимаб, адалимумаб, этанерсепт (воздействуют на фактор некроза опухоли (ФНО-α);
- ритуксимаб (воздействует на CD 20 (В-лимфоциты));
- анакинра (воздействует на интерлейкин-1);
- абатасепт (воздействует на CD 80, CD 86, CD 28).
Для биологических препаратов характерны выраженный клинический эффект и достоверно доказанное торможение деструкции суставов. Эти признаки позволяют относить биологические препараты к группе БПВП. В то же время особенностью группы является быстрое (нередко в течение нескольких дней) развитие яркого улучшения, что объединяет биологическую терапию с методами интенсивной терапии. Характерная черта биологических средств — потенцирование эффекта в сочетании с БПВП, в первую очередь с метотрексатом. В связи с высокой эффективностью при ревматоидном артрите, в том числе у резистентных к обычной терапии пациентов, в настоящее время биологическая терапия выдвинулась на второе по значимости место (после БПВП) в лечении этого заболевания.
К отрицательным сторонам биологической терапии относятся:
- угнетение противоинфекционного и (потенциально) противоопухолевого иммунитета;
- риск развития аллергических реакций и индуцирования аутоиммунных синдромов, связанный с тем, что биологические препараты по химической структуре являются белками;
- высокая стоимость лечения.
Биологические методы терапии показаны, если лечение препаратами из группы БПВП (такими, как метотрексат) не является адекватным вследствие недостаточной эффективности или неудовлетворительной переносимости.
Одной из наиболее важных молекул-мишеней служит ФНО-a, который имеет множество провоспалительных биологических эффектов и способствуют персистенции воспалительного процесса в синовиальной оболочке, деструкции хряща и костной ткани за счет прямого действия на синовиальные фибробласты, хондроциты и остеокласты. Блокаторы ФНО-α являются наиболее широко применяемыми биологическими средствами в мире.
В России зарегистрирован препарат из этой группы инфликсимаб (ремикейд), представляющий собой химерное моноклональное антитело к ФНО-α. Препарат, как правило, назначается в сочетании с метотрексатом. У пациентов с недостаточной эффективностью терапии средними и высокими дозами метотрексата инфликсимаб существенно улучшает ответ на лечение и функциональные показатели, а также приводит к выраженному торможению прогрессирования сужения суставной щели и развития эрозивного процесса.
Показанием к назначению инфликсимаба в комбинации с метотрексатом является неэффективность одного или более БПВП, применявшихся в полной дозе (в первую очередь метотрексата), с сохранением высокой воспалительной активности (пять и более припухших суставов, скорость оседания эритроцитов (СОЭ) более 30 мм/ч, С-реактивный белок (СРБ) более 20 мг/л). При раннем ревматоидном артрите с высокой воспалительной активностью и быстрым нарастанием структурных нарушений в суставах комбинированная терапия метотрексатом и инфликсимабом может быть назначена сразу.
До назначения инфликсимаба требуется провести скрининговое обследование на туберкулез (рентгенография грудной клетки, туберкулиновая проба). Рекомендуемая схема применения: начальная доза 3 мг/кг массы тела больного в/в капельно, затем по 3 мг/кг массы тела через 2, 6 и 8 нед, далее по 3 мг/кг массы тела каждые 8 нед, при недостаточной эффективности доза может повышаться вплоть до 10 мг/кг массы тела. Длительность лечения определяется индивидуально, обычно не менее 1 года. После отмены инфликсимаба поддерживающая терапия метотрексатом продолжается. Следует иметь в виду, что повторное назначение инфликсимаба после окончания курса лечения этим препаратом ассоциировано с повышенной вероятностью реакций гиперчувствительности замедленного типа.
Вторым зарегистрированным в нашей стране препаратом для проведения биологической терапии является ритуксимаб (мабтера). Действие ритуксимаба направлено на подавление В-лимфоцитов, которые не только являются ключевыми клетками, отвечающими за синтез аутоантител, но и выполняют важные регуляторные функции на ранних стадиях иммунных реакций. Препарат обладает выраженной клинической эффективностью, в том числе у больных, недостаточно отвечающих на терапию инфликсимабом.
Для лечения ревматоидного артрита препарат применяется в дозе 2000 мг на курс (две инфузии по 1000 мг, каждая с промежутком в 2 нед). Ритуксимаб вводится внутривенно медленно, рекомендуется проведение инфузии в условиях стационара с возможностью точного контроля за скоростью введения. Для профилактики инфузионных реакций целесообразно предварительное введение метилпреднизолона 100 мг. При необходимости возможно проведение повторного курса инфузий ритуксимаба через 6–12 мес.
Согласно европейским клиническим рекомендациям, ритуксимаб целесообразно назначать в случаях неэффективности или невозможности проведения терапии инфликсимабом. Возможность применения ритуксимаба в качестве первого биологического препарата служит в настоящее время предметом исследований.
Глюкокортикостероиды. Глюкокортикостероиды обладают многогранным противовоспалительным действием, обусловленным блокадой синтеза провоспалительных цитокинов и простагландинов, а также торможением пролиферации за счет воздействия на генетический аппарат клеток. Глюкокортикостероиды оказывают быстрый и ярко выраженный дозозависимый эффект в отношении клинических и лабораторных проявлений воспаления. Применение глюкокортикостероидов чревато развитием нежелательных реакций, частота которых также повышается с увеличением дозы препарата (стероидный остеопороз, медикаментозный синдром Иценко–Кушинга, поражение слизистой ЖКТ). Эти препараты сами по себе в большинстве случаев не могут обеспечить полноценного контроля над течением ревматоидного артрита и должны назначаться вместе с БПВП.
Глюкокортикостероиды при данном заболевании применяются системно и локально. Для системного применения показан основной метод лечения — назначение низких доз внутрь (преднизолон — до 10 мг/сут, метилпреднизолон — до 8 мг/сут) на длительный период при высокой воспалительной активности, полиартикулярном поражении, недостаточной эффективности БПВП.
Средние и высокие дозы глюкокортикостероидов внутрь (15 мг/сут и более, обычно 30–40 мг/сут в пересчете на преднизолон), а также пульс-терапия глюкокортикостероидами — внутривенное введение высоких доз метилпреднизолона (250–1000 мг) или дексаметазона (40–120 мг) могут применяться для лечения тяжелых системных проявлений ревматоидного артрита (выпотной серозит, гемолитическая анемия, кожный васкулит, лихорадка и др.), а также некоторых особых форм болезни. Продолжительность лечения определяется временем, необходимым для купирования симптоматики, и составляет обычно 4–6 нед, после чего осуществляется постепенное ступенчатое снижение дозы с переходом на лечение низкими дозами глюкокортикостероидов.
Глюкокортикостероиды в средних и высоких дозах, пульс-терапия, по-видимому, не обладают самостоятельным влиянием на течение ревматоидного артрита и развитие эрозивного процесса в суставах.
Для локальной терапии применяются препараты в микрокристаллической форме, назначающиеся в виде внутрисуставных и периартикулярных инъекций: бетаметазон, триамсинолон, метилпреднизолон, гидрокортизон.
Глюкокортикостероиды для локального применения обладают ярко выраженным противовоспалительным действием, преимущественно в месте введения, а в ряде случаев — и системным действием. Рекомендуемые суточные дозы составляют: 7 мг — для бетаметазона, 40 мг — для триамсинолона и метилпреднизолона, 125 мг — для гидрокортизона. Эта доза (суммарно) может использоваться для внутрисуставного введения в один крупный (коленный) сустав, два сустава среднего размера (локтевые, голеностопные и др.), 4–5 мелких суставов (пястно-фаланговые и др.), либо для периартикулярного введения препарата в 3–4 точки.
Эффект после однократного введения обычно наступает на протяжении 1–3 дней и сохраняется в течение 2–4 нед при хорошей переносимости.
В связи с этим повторные инъекции глюкокортикостероидов в один сустав нецелесообразно назначать ранее чем через 3–4 недели. Проведение курса из нескольких внутрисуставных инъекций в один и тот же сустав не имеет терапевтического смысла и чревато осложнениями (локальный остеопороз, усиление деструкции хряща, остеонекроз, нагноение). В связи с повышенным риском развития остеонекроза внутрисуставное введение глюкокортикостероидов в тазобедренный сустав в целом не рекомендуется.
Глюкокортикостероиды для локального применения назначаются в качестве дополнительного метода купирования обострений ревматоидного артрита и не могут служить заменой системной терапии.
НПВП. Значение НПВП в лечении ревматоидного артрита за последние годы существенно снизилось в связи с появлением новых эффективных схем патогенетической терапии. Противовоспалительное действие НПВП достигается с помощью подавления активности ЦОГ, или избирательно ЦОГ-2, и тем самым снижается синтез простагландинов. Таким образом НПВП действуют на конечное звено ревматоидного воспаления.
Действие НПВП при ревматоидном артрите — уменьшение выраженности симптомов болезни (боль, скованность, припухлость суставов). НПВП обладают обезболивающим, противовоспалительным, жаропонижающим эффектом, но мало влияют на лабораторные показатели воспаления. В подавляющем большинстве случаев НПВП не способны как-либо заметно изменить течение заболевания. Их назначение в качестве единственного противоревматического средства при достоверном диагнозе ревматоидный артрит в настоящее время считается ошибкой. Тем не менее НПВП являются основным средством симптоматической терапии при данном заболевании и в большинстве случаев назначаются в сочетании с БПВП.
Наряду с лечебным эффектом, все НПВП, включая селективные (ингибиторы ЦОГ-2), способны вызывать эрозивно-язвенное поражение ЖКТ (в первую очередь верхних его отделов — «НПВП-гастропатия») с возможными осложнениями (кровотечения, перфорации и пр.), а также нефротоксические и другие нежелательные реакции.
Основные характерные черты, которые необходимо учитывать при назначении НПВП, следующие.
- Не существует значимых различий между НПВП в плане эффективности (для большинства препаратов эффект пропорционален дозе вплоть до максимальной рекомендуемой).
- Существуют значительные различия между разными НПВП по переносимости, особенно в отношении поражения ЖКТ.
- Частота нежелательных эффектов обычно пропорциональна дозе НПВП.
- У пациентов с повышенным риском развития НПВП-ассоциированного поражения ЖКТ риск может быть снижен путем параллельного назначения блокаторов протонной помпы, мизопростола.
Существует индивидуальная чувствительность к различным НПВП как в отношении эффективности, так и переносимости лечения. Дозы НПВП при ревматоидном артрите соответствуют стандартным. Продолжительность лечения НПВП определяется индивидуально и зависит от потребности больного в симптоматической терапии. При хорошем ответе на терапию БПВП препарат из группы НПВП может быть отменен.
К наиболее часто применяющимся при ревматоидном артрите НПВП относятся:
- диклофенак (50–150 мг/сут);
- нимесулид (200–400 мг/сут);
- целекоксиб (200–400 мг/сут);
- мелоксикам (7,5–15 мг/сут);
- ибупрофен (800–2400 мг/сут);
- лорноксикам (8–12 мг/сут).
Селективные НПВП, по эффективности достоверно не отличаясь от неселективных, реже вызывают НПВП-гастропатии и серьезные нежелательные реакции со стороны ЖКТ, хотя и не исключают развитие этих осложнений. Ряд клинических исследований продемонстрировал повышенную вероятность развития тяжелой сосудистой патологии (инфаркт миокарда, инсульт) у пациентов, получавших препараты из группы коксибов, в связи с чем возможность лечения целекоксибом должна обсуждаться с особой осторожностью у больных с ИБС и другими серьезными кардиоваскулярными патологиями.
Дополнительные медикаментозные методы лечения. В качестве симптоматического анальгетика (или дополнительного анальгетика при недостаточной эффективности НПВП) может использоваться парацетамол (ацетаминофен) в дозе 500–1500 мг/сут, который обладает относительно невысокой токсичностью. Для локальной симптоматической терапии используются НПВП в виде гелей и мазей, а также диметилсульфоксид в виде 30–50% водного раствора в форме аппликаций. При наличии остеопороза показано соответствующее лечение препаратами кальция, витамина Д3, бифосфонатами, кальцитонином.
Общие принципы ведения больных РА
Больному с установленным диагнозом ревматоидный артрит должен быть назначен препарат из группы БПВП, который при хорошем клиническом эффекте может применяться как единственный метод терапии [9]. Другие лечебные средства используются по мере необходимости.
Больной должен быть информирован о характере своего заболевания, течении, прогнозе, необходимости длительного сложного лечения, а также о возможных нежелательных реакциях и схеме контроля за лечением, неблагоприятных сочетаниях с другими препаратами (в частности, алкоголем), возможной активации очагов хронической инфекции на фоне лечения, целесообразности временной отмены иммуносупрессивных препаратов при возникновении острых инфекционных заболеваний, о необходимости контрацепции на фоне лечения.
Терапия ревматоидного артрита должна назначаться врачом-ревматологом и проводиться под его наблюдением. Лечение биологическими препаратами может проводиться только под контролем ревматолога, имеющего достаточные знания и опыт для его проведения. Терапия является длительной и подразумевает периодический контроль активности болезни и оценку ответа на терапию. Упрощенный алгоритм представлен на рисунке 2.
Мониторинг активности болезни и ответа на терапию включает оценку показателей суставного статуса (число болезненных и припухших суставов и др.), острофазовых показателей крови (СОЭ, СРБ), оценку боли и активности болезни по визуальной аналоговой шкале, оценку функциональной активности больного в повседневной деятельности с помощью русского варианта опросника состояния здоровья (HAQ). Существуют признанные международным сообществом ревматологов методики количественной оценки ответа на лечение с помощью рекомендованного Европейской лигой по борьбе с ревматизмом (EULAR) индекса DAS (Disease Activity Score) и критериев Американской коллегии ревматологов (ACR) [1]. Кроме того, должен осуществляться мониторинг безопасности проводимой пациенту терапии (в соответствии и формуляром и существующими клиническими рекомендациями). В связи с тем, что эрозивный процесс может развиваться даже при низкой воспалительной активности, помимо оценки активности болезни и ответа на терапию обязательно применяется рентгенография суставов. Прогрессирование деструктивных изменений в суставах оценивают путем стандартной рентгенографии кистей и стоп с использованием рентгенологической классификации стадий ревматоидного артрита, количественных методик по индексам Sharp и Larsen. С целью мониторинга состояния больного обследование рекомендуется проводить с определенной периодичностью (табл. 2).
Лечение резистентного к терапии РА
Резистентным к лечению целесообразно считать пациента с неэффективностью (отсутствием 20% улучшения по основным показателям) как минимум двух стандартных БПВП в достаточно высоких дозах (метотрексат — 15–20 мг/нед, сульфасалазин — 2000 мг/сут, лефлуномид — 20 мг/сут). Неэффективность может быть первичной и вторичной (возникающей после периода удовлетворительного ответа на терапию либо при повторном назначении препарата). Существуют следующие пути преодоления резистентности к терапии:
- назначение биологических препаратов (инфликсимаб, ритуксимаб);
- назначение глюкокортикостероидов;
- применение комбинированной базисной терапии;
- применение БПВП второго ряда (циклоспорин и др.).
С точки зрения отдаленных результатов в отношении функциональных нарушений, качества жизни и ее продолжительности оптимальной стратегией терапии ревматоидного артрита является многолетнее лечение БПВП с планомерной сменой схемы их применения по мере необходимости [11].
Литература
- Клинические рекомендации. Ревматология/ под. ред. Е. Л. Насонова. М.: ГЭОТАР-Медиа, 2006. 288 с.
- Emery P., Suarez-Almazor M. Rheumatoid Arthritis// Clin Evid. 2003; 10: 1454–1476.
- Насонов Е. Л., Каратеев Д. Е., Чичасова Н. В., Чемерис Н. А. Современные стандарты фармакотерапии ревматоидного артрита// Клиническая фармакология и терапия. 2005. Т. 14. № 1. С. 72–75.
- Балабанова Р. М., Каратеев Д. Е., Кашеваров Р. Ю., Лучихина Е. Л. Лефлуномид (Арава) при раннем ревматоидном артрите// Научно-практическая ревматология. 2005. № 5. С. 31–34.
- Goekoop-Ruiterman Y. P., de Vries-Bouwstra J. K., Allaart C. F. et al. Clinical and radiographic outcomes of four different treatment strategies in patients with early rheumatoid arthritis (the BeSt study): a randomized, controlled trial// Arthritis Rheum. 2005; v. 52; 11: 3381–90.
- Smolen et al. Therapeutic strategies in early rheumatoid arthritis //Best Practice & Research Clinical Rheumatology. 2005; 19; 1: 163–177.
- Breeveld F. C., Emery P., Keystone E. et al. Infliximab in active early rheumatoid arthritis// Ann Rheum Dis 2004; 63: 149–155.
- Quinn M. A., Conaghan P. G., O’Connor P. J. et al. Very early treatment with infliximab in addition to methotrexate in early, poor-prognosis rheumatoid arthritis reduces magnetic resonance imaging evidence of synovitis and damage, with sustained benefit after infliximab withdrawal: results from a twelve-month randomized, double-blind, placebo-controlled trial// Arthritis Rheum. 2005; 52; 1: 27–35.
- American College of Rheumatology Subcommittee on Rheumatoid Arthritis Guidelines. Guidelines for the management of rheumatoid arthritis. 2002 Update// Arthritis Rheum. 2002; 46: 328–346.
- Quinn M. A., Emery P. Window of opportunity in early rheumatoid arthritis: possibility of altering the disease process with early intervention// Clin Exp Rheumatol. 2003; 21; Suppl 31: 154–157.
- Каратеев Д. Е. Ретроспективная оценка многолетней базисной терапии у больных ревматоидным артритом// Научно-практическая ревматология. 2003. № 3. С. 32–36.
Д. Е. Каратеев, доктор медицинских наук
Институт ревматологии РАМН, Москва
Комплексный анализ, используемый для оценки активности и контроля лечения ревматоидного артрита.
Синонимы русские
Анализы крови при ревматоидном артрите (РА).
Синонимы английские
Rheumatoid arthritis (RA) blood panel;
Rheumatoid arthritis laboratory tests;
Rheumatoid arthritis work up.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Детям в возрасте до 1 года не принимать пищу в течение 30-40 минут до исследования.
- Детям в возрасте от 1 до 5 лет не принимать пищу в течение 2-3 часов до исследования.
- Не принимать пищу в течение 12 часов до исследования, можно пить чистую негазированную воду.
- Полностью исключить (по согласованию с врачом) прием лекарственных препаратов в течение 24 часов перед исследованием.
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Ревматоидный артрит – это хроническое аутоиммунное заболевание, течение которого варьируется от незначительно выраженного олигоартрита до стремительной деструкции многих суставов и инвалидизации. Для оценки активности этого заболевания, его прогноза, принятия решения о назначении базисных препаратов и контроля лечения используют несколько клинико-лабораторных маркеров. Особенно удобным для врача и пациента является комплексный анализ крови, включающий все необходимые показатели.
Комплексный анализ крови при ревматоидном артрите состоит из 4 частей: маркеры воспаления, гематологические, биохимические и иммунологические показатели.
Маркеры воспаления – это скорость оседания эритроцитов (СОЭ), С-реативный белок (СРБ) и фибриноген. Высокий уровень СОЭ, СРБ или фибриногена отражает активность заболевания. Кроме того, было показано, что уровень СРБ связан с прогрессирующей деструкцией суставов по данным радиологического исследования. Фибриноген – это не только белок острой фазы воспаления, но и фактор свертывания крови, высокий уровень которого ассоциирован с риском тромбоза и сердечно-сосудистых заболеваний. Подобная ассоциация была показана и для СРБ. Действительно, риск сердечно-сосудистых заболеваний и инсульта у пациентов с ревматоидным артритом повышен.
Гематологические показатели – это общий анализ крови (ОАК) и лейкоцитарная формула. С помощью ОАК удается выявить и оценить степень выраженности анемии при ревматоидном артрите. При этом заболевании чаще всего наблюдается анемия хронических заболеваний, степень выраженности которой отражает активность заболевания. При хорошем ответе на терапию показатели крови нормализуются. Другой нередкой формой анемии является железодефицитная анемия, обусловленная скрытым кровотечением ЖКТ при применении НПВС. Для дифференциальной диагностики двух видов анемий при ревматоидном артрите могут понадобиться исследования уровня железа. Также с помощью ОАК можно выявить тромбоцитоз, который отражает активность заболевания, или тромбоцитопению, которая может возникнуть как осложнение при приеме лекарств или являться симптомом гиперспленизма при синдроме Фелти. При ревматоидном артрите, как правило, наблюдается умеренный лейкоцитоз. Лейкопения может возникать как осложнение при приеме лекарств или, по аналогии с тромбоцитопенией, являться симптомом синдрома Фелти.
К биохимическим показателям, которые исследуют при ревматоидном артрите, относятся печеночные ферменты (АЛТ, АСТ) и общий белок сыворотки крови. Печеночные ферменты исследуют для оценки гепатотоксичности, вероятной при назначении базисных препаратов, и своевременной коррекции их дозы. Повышение уровня печеночных ферментов наблюдается у 10-35 % пациентов, получающих комбинацию метотрексата и лефлуномида. Общий белок сыворотки – это интегральный показатель белкового обмена организма, который часто нарушается при хронических заболеваниях, в том числе при ревматоидном артрите. Следует отметить, что уровень общего белка может быть нормальным даже при тяжелом течении заболевания.
Иммунологические показатели – ревматоидный фактор (РФ) и антитела к циклическому цитруллинсодержащему пептиду (АЦЦП) – используют не только для диагностики, но и для оценки активности и прогноза ревматоидного артрита. РФ – это иммуноглобулины класса IgM к Fc-фрагменту иммуноглобулинов IgG. РФ выявляется у 60-80 % пациентов с ревматоидным артритом, чаще в стадию развернутой клинической картины. Чувствительность этого маркера на ранней стадии ревматоидного артрита составляет около 40 %. Таким образом, отрицательный результат исследования РФ не позволяет полностью исключить ревматоидный артрит. Уровень РФ в некоторой степени меняется с изменением активности заболевания, но может оставаться высоким даже при достижении клинической ремиссии заболевания. Наличие РФ связано с прогрессирующей деструкцией суставов по данным рентгенологического исследования вне зависимости от активности заболевания. РФ не является специфичным для ревматоидного артрита маркером и может быть обнаружен при многих других аутоиммунных заболеваниях, в том числе при системной красной волчанке, анкилозирующем спондилите, ювенильном ревматоидной артрите, саркоидозе, а также определяется у 5-7 % здоровых людей. Более специфичным маркером ревматоидного артрита являются антитела к циклическому цитруллинсодержащему пептиду (АЦЦП), IgG. АЦЦП – это гетерогенная группа аутоантител, взаимодействующих с аминокислотой цитруллином различных белков (возможно, фибрина, виментина, коллагена I и II типа, гистонов и других), образующейся в результате воспалительных изменений в суставе. Специфичность этого маркера достигает 99 %. Также АЦЦП чаще, чем РФ (60 % по сравнению с 40 %), наблюдаются на ранней стадии ревматоидного артрита. Считается, что концентрация АЦЦП может отражать активность заболевания. Обнаружение АЦЦП, подобно РФ, ассоциировано с деструкцией суставов и является неблагоприятным прогностическим фактором.
В некоторых случаях могут понадобиться дополнительные тесты, например анализ кала на скрытую кровь у пациента, принимающего НПВС, или оценка функции почек у пациента, принимающего метотрексат. Следует отметить, что лабораторное обследование – важное, но не единственное обследование при ревматоидном артрите. Результаты комплексного анализа необходимо оценивать с учетом дополнительных анамнестических, клинических и инструментальных данных.
Для чего используется исследование?
- Для оценки активности и контроля лечения ревматоидного артрита.
Когда назначается исследование?
- При наличии симптомов поражения суставов: боли и ограничения подвижности (скованности) в суставах, отек и покраснение кожи в области суставов, особенно при симметричном поражении мелких суставов кистей и стоп;
- при контрольном обследовании пациента с ревматоидным артритом.
Что означают результаты?
Референсные значения
Для каждого показателя, входящего в состав комплекса:
- [02-005] Клинический анализ крови (c лейкоцитарной формулой)
- [02-007] Скорость оседания эритроцитов (СОЭ)
- [06-182] С-реактивный белок, количественно (метод с нормальной чувствительностью)
- [13-020] Ревматоидный фактор
- [13-026] Антитела к цитруллинированному виментину (анти-MCV)